I. TÓM TẮT LÍ THUYẾT
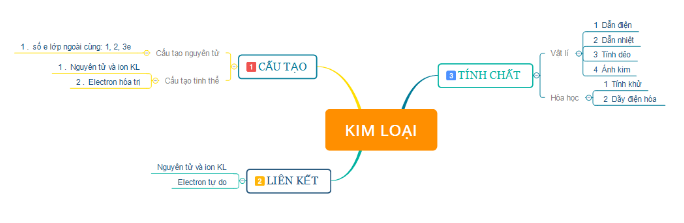
II.GIẢI BÀI TẬP SÁCH GIÁO KHOA
Câu 1. (Trang 100 SGK)
Có 4 ion là Ca2+, Al3+, Fe2+, Fe3+. Ion có số electron ở lớp ngoài cùng nhiều nhất là
A. Fe3+
B. Fe2+
C. Al3+
D. Ca2+
Bài làm:
Đáp án B
Ion có số electron ở lớp ngoài cùng nhiều nhất là Fe2+
Câu 2. (Trang 100 SGK)
Kim loại có tính chất vật lí chung là dẫn điện, dẫn nhiệt, dẻo và có ánh kim. Nguyên nhân của những tính chất vật lí chung của kim loại là do trong tinh thể kim loại có
A. nhiều electron độc thân.
B. các ion dương chuyển động tự do.
C. các electron chuyển động tự do.
D. nhiều ion dương kim loại.
Bài làm:
Đáp án C
Kim loại có tính chất vật lí chung là dẫn điện, dẫn nhiệt, dẻo và có ánh kim. Nguyên nhân của những tính chất vật lí chung của kim loại là do trong tinh thể kim loại có các electron chuyển động tự do.
Câu 3. (Trang 100 SGK)
Kim loại khác nhau có độ dẫn điện, dẫn nhiệt khác nhau. Sự khác nhau đó được quyết định bởi
A. khối lượng riêng khác nhau.
B. kiểu mạng tinh thể khác nhau.
C. mật độ electron tự do khác nhau.
D. mật độ ion dương khác nhau.
Bài làm:
Đáp án C
Kim loại khác nhau có độ dẫn điện, dẫn nhiệt khác nhau. Sự khác nhau đó được quyết định bởi mật độ electron tự do khác nhau.
Câu 4. (Trang 100 SGK)
Ngâm một lá kim loại Ni trong những dung dịch muối sau: MgSO4, NaCl, CuSO4, AlCl3, ZnCl2, Pb(NO3)2, AgNO3. Hãy cho biết muối nào có phản ứng với Ni. Giải thích và viết phương trình hoá học.
Bài làm:
Các muối phản ứng với Ni là: CuSO4, Pb(NO3)2, AgNO3.
PTHH:
Ni + CuSO4 → NiSO4 + Cu↓
Ni + Pb(NO3)2 → Ni(NO3)2 + Pb↓
Ni + 2AgNO3 → Ni(NO3)2 + 2Ag
Câu 5. (Trang 101 SGK)
Để làm sạch một mẫu thuỷ ngân có lẫn tạp chất là kẽm, thiếc, chì người ta khuấy mẫu thuỷ ngân này trong dung dịch HgSO4 dư.
a) Hãy giải thích phương pháp làm sạch và viết các phương trình hoá học.
b) Nếu bạc có lẫn tạp chất là các kim loại nói trên, bằng phương pháp nào có thể loại được tạp chất? Viết phương trình hoá học.
Bài làm:
a) Do kẽm, thiếc, chì là cá kim loại mạnh hơn thủy ngân, nên khi tác dụng với dung dịch muối thủy ngân các kim loại này sẽ đẩy ion thủy ngân ra khỏi muối. Như vậy mẫu Hg không còn lẫn tạp chất nữa.
Zn + HgSO4 → ZnSO4 + Hg
Sn + HgSO4 → SnSO4 + Hg
Pb + HgSO4 → PbSO4 + Hg
b) Tương tự với bạc, ta sẽ cho mẫu bạc này ngâm trong dung dịch AgNO3 dư để loại bỏ tạp chất.
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
Sn + 2AgNO3 → Sn(NO3)2 + 2Ag
Pb + 2AgNO3 → Pb(NO3)2 + 2Ag
Câu 6. (Trang 101 SGK)
Hoà tan hoàn toàn 20 gam hỗn hợp Fe và Mg trong dung dịch HCl thu được 1 gam khí H2. Khi cô cạn dung dịch thu được bao nhiêu gam muối khan?
A. 54,5 gam,
B. 55,5 gam,
C. 56,5 gam,
D. 57,5 gam.
Bài làm:
Đáp án B
Ta có: nH2 = 1 / 2 = 0,5 (mol)
Bảo toàn nguyên tố H => nH+ = 2. 0,5 = 1 (mol) => nCl- = 1 mol
Khối lượng muối
mmuối = mkim loại + mgốc axit = 20 + 35,5.1 = 55,5 (gam)
Câu 7. (Trang 101 SGK)
Hoà tan hoàn toàn 0,5 gam hỗn hợp gồm Fe và một kim loại hoá trị II trong dung dịch HCl thu được 1,12 lít H2 ở dktc. Kim loại M là
A. Mg.
B. Ca.
C. Zn.
D. Be.
Bài làm:
Đáp án D
nH2 = 1,12 / 22,4 = 0,05 mol
=> Mtrung bình của hỗn hợp = 0,5/0,05 = 10 (g)
=>Kim loại đó là Be
Câu 8. (Trang 100 SGK)
Cho 16,2 gam kim loại M có hoá trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hoà tan vào dung dịch HCl dư thấy thoát ra 13,44 lít H2 ở đktc. Kim loại M là
A. Fe.
B. Al.
C. Ca.
D. Mg.
Bài làm:
Đáp án B
Ta có: nH2 = 13,44/22,4 = 0,6 mol
M → Mn+ + ne
1,8/n 1,8
O2 + 4e → 2O2-
0,15 0,6
2H+ + 2e → H2
1,2 0,6
Từ các bán phản ứng =>nM = 1,8/n (mol)
=>MM = 16,2.n/1,8 = 9n
=>Với n = 3 thì MM = 27 => Kim loại M là nhôm (Al = 27)
Câu 9. (Trang 101 SGK)
Có 5 kim loại là Mg, Ba, Al, Fe, Ag. Nếu chỉ dùng thêm dung dịch H2SO4 loãng thì có thể nhận biết được các kim
A. Mg, Ba, Ag.
B. Mg, Ba, Al.
C. Mg, Ba, Al, Fe.
D. Mg, Ba, Al, Fe, Ag.
Bài làm:
Đáp án D
Ag không tan trong dung dịch H2SO4 loãng.
Ba tạo kết tủa với dung dịch H2SO4 loãng.
Fe, Al, Mg tan trong dung dịch H2SO4 loãng.
Hòa tan Ba vào nước được Ba(OH)2.
Al tan trong Ba(OH)2 dư. Sắt tạo kết tủa trắng xanh để một thời gian hóa nâu , còn magie tạo kết tủa trắng.
Câu 10. (Trang 100 SGK)
Cho bột Cu dư vào dung dịch hỗn hợp gồm Fe(NO3)3 và AgNO3. Sau phản ứng kết thúc thu được chất rắn A và dung dịch B. Viết phương trình hoá học của các phản ứng xảy ra và cho biết A, B gồm những chất gì, biết rằng:
Tính oxi hoá: Ag+ > Fe3+ > Cu2+ > Fe2+.
Tính khử: Cu > Fe2+ > Ag.
Bài làm:
Cho Cu dư vào xảy ra phản ứng:
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Cu + 2Fe(NO3)3 → 2Fe(NO3)2 + Cu(NO3)2
=> Chất rắn A gồm Ag và Cu dư.
Dung dịch B chứa các muối Fe(NO3)2 và Cu(NO3)2







