I. Khái niệm, phân loại, đồng phân, danh pháp
1. Khái niệm: Khi thay thế 1 hay nhiều nguyên tử hidro trong phân tử hidrocacbon bằng 1 hay nhiều nguyên tử halogen ta được dẫn xuất halogen
2. Phân loại
- Dựa vào loại halogen có: dẫn xuất flo, dẫn xuất clo, dẫn xuất brom, dẫn xuất iot, dẫn xuất chứa đồng thời một vài halogen khác nhau.
- Dựa theo cấu tạo của gốc:
+ Dẫn xuất halogen no: CH2FCl, CH2-Cl-CH2Cl, CH3-CHBr-CH3....
+ Dẫn xuất halogen không no: CF2=CF2, CH2=CH-Cl, CH2=CH-CH2Br...
+ Dẫn xuất halogen thơm: C6H5F, C6H5CH2Cl, C6H5I...
- Dựa theo bậc của cacbon: bậc của dẫn xuất halogen chính là bậc của nguyên tử C liên kết trực tiếp với nguyên tử halogen
+ Dẫn xuất halogen bậc I: CH3CH2Cl (etyl clorua)
+ Dẫn xuất halogen bậc II: CH3CHClCH3 (isopropyl clorua)
+ Dẫn xuất halogen bậc III: (CH3)C-Br (tert - butyl bromua)
3. Đồng phân và danh pháp
a. Đồng phân: dẫn xuất halogen có đồng phân mạch cacbon và đồng phân vị trí nhóm chức
b. Tên thông thường:
CHCl3 (clorofom), CHBr3(bromofom) , CHI3 (iodofom)
c. Tên gốc-chức:
CH2=CH-Cl (vinyl clorua); CH2=CH-CH2-Cl (anlyl clorua); C6H5CH2Cl (benzyl clorua)
d. Tên thay thế: coi các nguyên tử halogen là các nhóm thế
CH2-Cl-CH2Cl (1,2-dicloetan) CHCl3 (triclometan)
II. Tính chất vật lý
- Ở điều kiện thường các dẫn xuất monohalogen có phân tử khối nhỏ là những chất khí
- Các dẫn xuất halogen không tan trong nước tan trong dung môi phân cực: hidrocacbon, ete
- Nhiều dẫn xuất halogen có hoạt tính sinh học cao CHCl3 có tác dụng gây mê, C6H6Cl6 diệt sâu bọ
III. Tính chất hóa học
1. Phản ứng thế nguyên tử halogen bằng nhóm - OH
a. Dẫn xuất ankyl halogenua
R – X + NaOH R – OH + NaX
C2H5 – Br + NaOH C2H5 – OH + NaBr
2. Phản ứng tách hidro halogenua
- CH3-CH2Cl + KOH to → CH2=CH2 + KCl + H2O
- PTTQ: (đối với dẫn xuất halogen no, đơn chức, mạch hở)
CnH2n+1X + KOH to → CnH2n + KX + H2O
- Quy tắc Zaixep: Nguyên tử X tách ra cùng với nguyên tử H ở C bậc cao hơn bên cạnh.
BÀI TẬP
Bài 1 (Trang 177 – SGK)
Gọi tên mỗi chất sau: CH3-CH2Cl, CH2=CH-CH2Cl, CHCl3. C6H5Cl. Viết phương trình hoá học của các phản ứng điều chế mỗi chất trên từ hiđrocacbon tương ứng.
Lời giải
.png)
Điều chế:
CH3-CH3 + Cl2 -as, 1:1→ CH3-CH2Cl + HCl
CH2=CH-CH3 + Cl2 -as, to→ CH2=CH-CH2Cl + HCl
CH4 + 3Cl2 -as, 1:1→ CHCl3 + 3HCl
C6H6 + Cl2 -Fe, to→ C6H5Cl + HCl
Bài 2 (Trang 177 – SGk)
Viết phương trình hoá học của phản ứng thuỷ phân các chất sau trong dung dịch NaOH: 1,2- đicloetan; benzylclorua; antyl bromua; xiclohexyl clorua.
Lời giải
Phương trình phản ứng theo thứ tự các chất:
Cl-CH2-CH2-Cl + 2NaOH → OH-CH2-CH2-OH + 2NaCl
C6H5-CH2-Cl + NaOH → C6H5-CH2-OH + NaCl
CH2=CH-CH2-Br + NaOH → CH2=CH-CH2-OH + NaBr
C6H11-Cl + NaOH → C6H11-OH + NaCl
Phương trình phản ứng theo CTCT:
.png)
Bài 3 (Trang 177 – SGK)
Cho nhiệt độ sôi (oC) của một số dẫn xuất halogen trong bảng dưới đây:
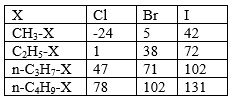
Nhận xét về sự biến đổi nhiệt độ sôi theo chiều tăng mạch cacbon (theo hàng dọc) và theo nguyên tử khối của halogen (hàng ngang). Giải thích sơ bộ.
Lời giải
– Theo chiều tăng mạch cacbon (hàng dọc), nguyên từ khối tăng nhiệt độ sôi của các chất tăng dần.
- Khi nguyên tử khối tăng (theo hàng ngang), nhiệt độ sôi cùng giảm dần.
- Khi nguyên tử khối tăng cần tốn nhiều năng lượng để chuyển các phân tử hữu cơ sang trạng thái hơi nhiệt độ sôi tăng.
Bài 4 (Trang 177 – SGK)
Từ axetilen, viết phương trình hoá học của các phản ứng điều chế: etyl bromua (1); 1,2-đibrometan (2); vinyl clorua (3); 1,1-đibrometan (4).
Lời giải
.png)
Bài 5 (Trang 177 – SGK)
Dùng hai ống nghiệm, mỗi ống đựng 1ml một chất lỏng sau: etyl bromua (1), brombenzen (2). Thêm tiếp vào mỗi ống 1 ml dung dịch AgNO3. Đun sôi hai ống nghiệm thấy ở (1) có kết tủa vàng nhạt, trong khi đó ở ống (2) không có hiện tượng gì. Nhận xét, giải thích các hiện tượng thí nghiệm trên?
Lời giải
.png)
Bài 6 (Trang 177 – SGK)
Khi đun nóng etyl clorua trong dung dịch chứa KOH và C2H5OH, thu được:
A. Etanol ; B. Etilen
C. Axetilen ; D. Etan
Lời giải
- Đáp án B
.png)







