BENZEN VÀ ĐỒNG ĐẲNG
I. Đồng đẳng, đồng phân, danh pháp, cấu tạo
1. Dãy đồng đẳng của benzen
- C6H6 (benzen), C7H8 (toluen), C8H10, ... ,
- CTTQ: CnH2n-6(n ≥ 6, nguyên)
2. Đồng phân, danh pháp
Đồng phân
C6H6 và C7H8 không có đồng phân hidrocacbon thơm.
Từ C8H10 trở đi có
- Đồng phân vị trí tương đối của các nhóm ankyl (các vị trí o, m, p)
- Đồng phân cấu tạo mạch cacbon của nhánh
Danh pháp
Tên hệ thống: nhóm ankyl + benzen
Chú ý: Nếu vòng benzen liên kết với nhiều nhóm ankyl tên gọi: số chỉ vị trí nhánh + tên nhánh + benzen
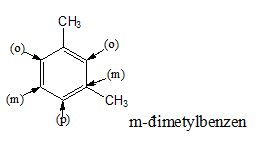
Cách đánh số các nguyên tử C trong vòng benzen sao cho tổng chỉ số trong tên gọi là nhỏ nhất.

3. Cấu tạo

Có hai cách biểu diễn công thức của benzen:
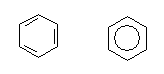
II. Tính chất vật lí
- Các hiđrocacbon thơm đều là chất lỏng hoặc rắn ở điều kiện thường ; ts, tnc tăng theo chiều tăng của phân tử khối.
- Hiđrocacbon thơm ở thể lỏng có mùi đặc trưng, không tan trong nước, nhẹ hơn nước, hòa tan được nhiều chất hữu cơ.
III. Tính chất hóa học
1. Phản ứng thế
a) Thế nguyên tử H của vòng benzen
*Phản ứng với halogen
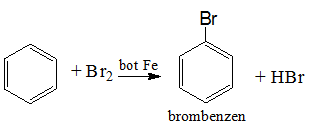
- Benzen phản ứng thế với brom
Toluen tác dụng với brom
.png)
Phản ứng với axit nitric
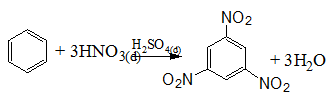
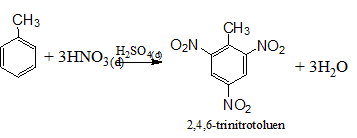
Quy tắc thế ở vòng benzen:
- Khi ở vòng benzen đã có sẵn nhóm ankyl (hay các nhóm –OH, -NH2, -OCH3,...), phản ứng thế vào vòng sẽ dễ dàng hơn và ưu tiên thế vào vị trí o-, p-.
- Nếu vòng benzen đã có sẵn nhóm –NO2 ( hoặc các nhóm –COOH, -SO3H, ...) phản ứng thế vào vòng sẽ khó hơn và ưu tiên xảy ra ở vị trí m-.
b) Thế nguyên tử H của mạch nhánh
2. Phản ứng cộng
a) Cộng hidro
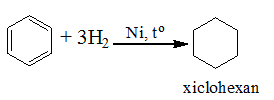
b) Cộng clo

3 Phản ứng oxi hóa
Phản ứng oxi hóa không hoàn toàn

Phản ứng oxi hóa hoàn toàn
CnH2n – 6 + 3n−32O2→(to) nCO2 + (n-3)H2O
HIĐROCACBON THƠM KHÁC
1. Cấu tạo
- Stiren có CTPT: C8H8
- CTCT:
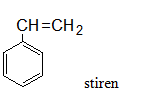
2. Tính chất hóa học
- Phản ứng cộng

- Phản ứng trùng hợp
.png)
- Phản ứng oxi hóa

ỨNG DỤNG CỦA MỘT SỐ HIĐROCACBON THƠM

Bài 1 (Trang 159 – SGK)
Ứng với công thức phân tử C8H10 có bao nhiêu đồng phân hiđrocacbon thơm?
A. 2 ; B. 3
C. 4 ; D. 5
Hãy chọn đáp án đúng
Lời giải
- Đáp án C
- 4 đồng phân hiđrocacbon thơm của C8H10 là:
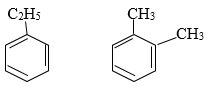

Bài 2 (Trang 159 – SGk)
Toluen và benzen cùng phản ứng được với chất nào sau đây: (1) dung dịch brom trong CCl4; (2) dung dịch kali pemanganat; (3) hiđro có xúc tác Ni, đun nóng; (4)Br2 có bột Fe, đun nóng? Viết phương trình hoá học của các phương trình xảy ra.
Lời giải
.png)
Bài 3 (Trang 159 – SGK)
Viết phương trình hoá học của các phản ứng xảy ra trong mỗi trường hợp sau:
a. Toluen tác dụng với hiđro có xúc tác Ni, áp suất cao, đun nóng.
b. Đun nóng benzen với hỗn hợp HNO3 đặc và H2SO4 đặc.
Lời giải
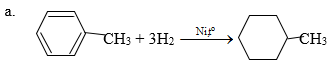
.png)
Bài 4 (Trang 159 – SGK)
Trình bày phương pháp hoá học phân biệt các chất: benzen, hex-1-en và toluen. Viết phương trình hoá học của các phản ứng đã dùng
Lời giải
- Cho các chất lần lượt tác dụng với dung dịch Br2, chất nào làm nhạt màu dung dịch Br2 thì đó là hex-1-en.
- Cho 2 chất còn lại qua dung dịch KMnO4, chất nào làm mất màu dung dịch KMnO4 thì đó là toluen.

Bài 5 (Trang 160 – SGK)
Hiđrocacbon X là chất lỏng có tỉ khối hơi so với không khí bằng 3,17. Đốt cháy hoàn toàn thu được CO2 có khối lượng bằng 4,28 lần khối lượng của nước. Ở nhiệt độ thường, X không làm mất màu dung dịch brom; khi đun nóng, X làm mất màu KMnO4.
a. Tìm công thức phân tử và viết công thức cấu tạo của X?
b. Viết phương trình hoá học của phản ứng giữa X với H2 (xúc tác Ni, đun nóng), với brom (có mặt bột Fe), với hỗn hợp dư của axit HNO3 và axit H2SO4 đậm đặc.
Lời giải
MX = 3,17. 29 = 92 ⇒ 12x + y = 92 (1)
Gọi CTPT của X là CxHy:
CxHy + (x + y/4)O2 → xCO2 + (y/2)H2O
mCO2 = 4,28mH2O ↔ 44x = 4,28. 18. (y/2) ⇒ y = 1,14x (2)
Từ (1) và (2) ⇒ x = 7, y = 8. CTPT của X là C7H8
Từ đề bài ⇒ CTCT của X là:

.png)
.png)
.png)
Bài 6 ( Trang 160 – SGK)
Đánh dấu (+) vào ô cặp chất phản ứng với nhau theo mẫu sau:

Lời giải

Bài 7 (Trang 160 – SGk)
Cho benzen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế nitrobenzen. Tính khối lượng nitrobenzen thu được khi dùng 1,00 tấn benzen với hiệu suất 78,0%.
Lời giải
Phương trình phản ứng:
C6H6 + HNO3 -H2SO4→ C6H5NO2 + H2O
Theo pt: 78(g) 123(g)
Theo đb: 106. 78%(g) x(g)
Do H = 78% nên lượng nitro benzen thu được là:
\[\Rightarrow x=\frac{{{10}^{6}}.78{\scriptstyle{}^{0}/{}_{0}}.123}{78}=1,{{26.10}^{6}}\,(g)\,=1,23\] (tấn)
Bài 8 ( Trang 160 – SGk)
So sánh tính chất hoá học của etylbenzen với stiren, viết phương trình hoá học của phản ứng để minh hoạ.
Lời giải
a. Giống nhau: đều phản ứng thế
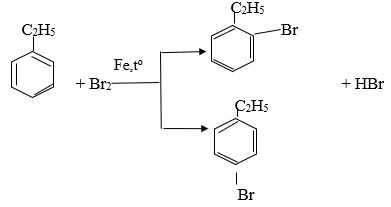
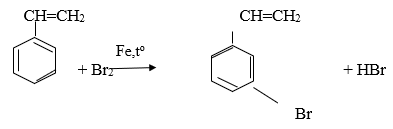
b. Khác nhau:
Etylbenzen có tính chất giống ankan

Stiren có tính chất giống anken

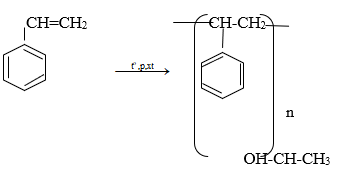
Bài 9 (Trang 160 – SGK)
Dùng công thức cấu tạo viết phương trình hoá học của stiren với:
a. H2O( xúc tác H2SO4)
b. HBr
c. H2 (theo tỉ lệ mol 1:1, xúc tác Ni)
Lời giải
.png)
Bài 10 (Trang 160 – SGk)
Trình bày phương pháp hoá học phân biệt 3 chất lỏng sau: toluen, benzen, stiren. Viết phương trình hoá học của các phản ứng hoá học đã dùng.
Lời giải
- Cho 3 chất lỏng tác dụng với dung dịch KMnO4 ở nhiệt độ thường, chất nào làm mất màu dung dịch KMnO4 ở nhiệt độ thường là stiren.
- Với 2 hỗn hợp phản ứng còn lại ta đem đun nóng, chất nào làm mất màu dung dịch KMnO4 (nóng) thì là toluen, còn lại là benzen.
.png)
Bài 11 (Trang 160 – SGK)
Khi tách hiđro của 66,25 kg etylbenzen thu được 52,00 kg stiren. Tiến hành phản ứng trùng hợp toàn bộ lượng stiren này thu được hỗn hợp A gồm polistiren và phần stiren chưa tham gia phản ứng. Biết 5,20 gam A vừa đủ làm mất màu của 60,00 ml dung dịch brom 0,15M.
a. Tính hiệu suất của phản ứng tách hiđro của etylbenzen.
b. Tính khối lượng stiren đã trùng hợp.
c. Polistren có phân tử khối trung bình bằng 3,12.105. Tính hệ số trùng hợp trung bình của polime.
Lời giải
.png)
Theo định luật bảo toàn khối lượng: \[{{m}_{A}}={{m}_{stiren}}=52,00\,(kg)\,={{52.10}^{3}}\,(g)\]
Theo đề bài: 5,2 g A tác dụng vừa đủ với 0,009 mol Br2
\[\Rightarrow \]\[{{52.10}^{3}}\]g A tác dụng vừa đủ với 90 mol Br2
Theo (3): \[{{n}_{_{stiren}}}={{n}_{B{{r}_{2}}}}=90\,(mol)\]
\[\Rightarrow {{m}_{stiren}}=90.104=9360\,(g)=9,36\,(kg)\]
Khối lượng stiren đã tham gia trùng hợp là : \[{{m}_{A}}-{{m}_{stiren}}=52-9,36=42,64\,(kg)\]
c. Hệ số trùng hợp là : \[n=\frac{312000}{104}=3000\]
Bài 12 (Trang 161– SGK)
Trình bày cách đơn giản để thu được naphtalen tinh khiết từ hỗn hợp naphtalen có lẫn tạp chất không tan trong nước và không bay hơi.
Lời giải
Úp miệng phễu có gắn giấy đục lỗ trên hỗn hợp naphtalen và tạp chất, đun nóng (lắp dụng cụ như hình 7.3/Sách giáo khoa trang 157), naphtalen thăng hoa tạo các tinh thể hình kim bám trên mặt giấy, ta thu được naphtalen tinh khiết.
Bài 13 (Trang 161 – SGK)
Từ etilen và benzen, tổng hợp được stiren theo sơ đồ:
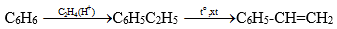
a. Viết các phương trình hoá học thực hiện sự biến đổi trên?
b. Tính khối lượng stiren thu được từ 1,00 tấn benzen nếu hiệu suất của quá trình là 78%.
Lời giải
.png)
Theo phương trình phản ứng: nstiren = nbenzen
Nhưng do hiệu suất = 78,00%
\[\Rightarrow {{n}_{stiren}}={{n}_{{{C}_{6}}{{H}_{6}}}}=\frac{{{1.10}^{6}}}{78}.\frac{78}{100}={{1.10}^{4}}\,(mol)\]
\[\Rightarrow \] Khối lượng stiren = 1.104.104(g) = 1,04 (tấn)







