I. Đồng đẳng, đồng phân, danh pháp
1. Dãy đồng đẳng anken: (olefin)
Anken là các hidrocacbon mạch hở, trong phân tử có 1 liên kết đôi.
Công thức chung : CnH2n với n ≥ 2.
2. Đồng phân
Đồng phân cấu tạo: Bắt dầu từ C4H8 trở đi có đồng phân anken.
- Đồng phân về vị trí nối đôi.
- Đồng phân về mạch cacbon.
Đồng phân hình học:
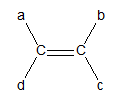
- Điều kiện để có đồng phân hình học là a ≠ d và b ≠ c.
- Đồng phân hình học có mạch chính nằm cùng một phía của liên kết đôi gọi là cis, ngược lại gọi là trans.
3. Danh pháp
- Tên thông thường: Tên mạch C chính + ilen
- Tên thay thế (danh pháp IUPAC):
Mạch không phân nhánh: Tên mạch C chính + số chỉ vị trí nối đôi + EN
Mạch phân nhánh
Quy tắc:
- Chọn mạch C dài nhất chứa nối đôi làm mạch chính.
- Đánh STT trên mạch C chính, ưu tiên C mang nối đôi có STT nhỏ nhất, nếu mạch vừa có nhánh vừa có nối đôi thì ưu tiên một là vị trí nối đôi kế đó là vị trí nhánh thì ưu tiên hai.
- Gọi tên anken phân nhánh :
Số chỉ vị trí-tên nhánh + tên mạch C chính + số chỉ trí nối đôi + EN
II. Tính chất vật lí
- Từ C2 - C4 : khí , C5 trở đi : rắn hoặc lỏng.
- M tăng tso, tnco, khối lượng riêng tăng.
- Các anken là những chất nhẹ hơn nước và không tan trong nước.
III. Tính chất hóa học
1. Phản ứng cộng
- Cộng hiđrô : (Phản ứng hiđro hoá)
CnH2n + H2 →(to) CnH2n+2
- Cộng halogen : (Phản ứng halogen hoá)
CH2=CH2 + Br2 → BrCH2 - CH2Br
(Màu nâu đỏ) 1,2-đibrometan (Không màu)
CnH2n + Br2 → CnH2nBr2
\[\Rightarrow \] Anken làm mất màu của dung dịch brom → Phản ứng này dùng để nhận biết anken .
- Cộng HX (X là OH, Cl, Br,…)
Qui tắc Mac-côp-nhi-côp:
Trong phản ứng cộng HX vào liên kết đôi, nguyên tử H (hay phần mang điện tích dương) chủ yếu cộng vào nguyên tử cacbon bậc thấp hơn (có nhiều H hơn), còn nguyên tử hay nhóm nguyên tử X (phần mang điện tích âm) cộng vào nguyên tử cacbon bậc cao hơn (có ít H hơn).
Ví dụ :
CH3-CH=CH2 + HBr → CH3-CH2-CH2Br (sản phẩm phụ)
CH3-CH=CH2 + HBr → CH3-CH(Br)-CH3 (sẩn phẩm chính)
2. Phản ứng trùng hợp
nCH2=CH2 →(to, xt, p) [- CH2–CH2 -]n
- Phản ứng trùng hợp là quá trình kết hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau tạo thành những phân tử rất lớn gọi là polime .
Tên polime = poli + tên monome
3. Phản ứng oxi hoá
Oxi hoá hoàn toàn
CnH2n + O2 →(to) nCO2+ nH2O
Oxi hoá không hoàn toàn
3CH2=CH2 + 4H2O + 2KMnO4 → 3HO-CH2-CH2-OH + 2MnO2 + 2KOH
\[\Rightarrow \]Anken làm mất màu dd KMnO4 → Dùng để nhận biết anken
IV. Điều chế
1. Trong PTN
C2H5OH →(H2SO4 đ, 170oC) CH2 = CH2 + H2
2. Trong công nghiệp
CnH2n+2 →(to, xt, p) CnH2n + H2
V. Ứng dụng

Bài 1 (Trang 132 – SGK)
So sánh anken với ankan về đặc điểm cấu tạo và tính chất hóa học. Cho thí dụ minh họa.
Bài giải
- Về đặc điểm cấu tạo: Khác với ankan là phân tử chỉ chứa liên kết σ, phân tử anken còn có chứa 1 liên kết π kém bền, dễ gẫy.
- Do đó về tính chất hóa học cũng không giống với ankan là cho phản ứng thế là phản ứng đặc trưng, anken cho phản ứng cộng là phản ứng đặc trưng
Ví dụ:
C2H4 + H2→C2H6 (xúc tác : Ni)
C2H4 + Br2→C2H4Br2
C2H4 + HBr→C2H5Br
Ngoài ra anken còn cho phản ứng trùng hợp phản ứng làm mất màu dung dịch thuốc tím.
Ví dụ :
\[3{{C}_{2}}{{H}_{4}}+2KMn{{O}_{4}}+4{{H}_{2}}O\to 2{{C}_{2}}{{H}_{4}}{{\left( OH \right)}_{2}}+2Mn{{O}_{2}}+2K\text{O}H\]
\[nC{{H}_{2}}=C{{H}_{2}}\xrightarrow{xt,{{t}^{0}},p}{{\left( -C{{H}_{2}}-C{{H}_{2}}- \right)}_{n}}\]
Bài 2 (Trang 132 – sGK)
Ứng với công thức C5H10 có bao nhiêu đồng phân cấu tạo ?
A. 4 ; B. 5 ; C. 3 ; D. 7
Bài giải
- Đáp án B
- Các công thức cấu tạo:
.png)
Bài 3 (Trang 132 – SGK)
Viết phương trình hóa học của phản ứng xảy ra khi:
a. Propilen tác dụng với hidro, đun nóng (xúc tác Ni).
b. But-2-en tác dụng với hirdo clorua.
c. Metylpropen tác dụng với nước có xúc tác axit.
d. Trùng hợp but-1-en.
Bài giải
a) \[C{{H}_{3}}-CH=C{{H}_{2}}+{{H}_{2}}\xrightarrow{Ni,{{t}^{0}}}C{{H}_{3}}-C{{H}_{2}}-C{{H}_{3}}\]
.png)







