A. KIẾN THỨC CẦN NHỚ
I. Dạng thù hình là gì?
Dạng thù hình của một nguyên tố là những đơn chất khác nhau do cùng một nguyên tố tạo nên.
Thí dụ oxi O2, ozon O3 là hai dạng thù hình của nguyên tố oxi.
Những nguyên tố có thể tồn tại tự do với vài dạng đơn chất gọi là nguyên tô có tính thù hình.
II. Cacbon có những dạng thù hình nào?
Nguyên tố cacbon có 3 dạng thù hình là:
- Kim cương: cứng, trong suốt, không dẫn điện.
- Than chì: mềm, dẫn điện.
- Cacbon vô định hình (than đá, than gỗ, than xương): xốp, không dẫn điện.
III. TÍNH CHẤT CỦA CACBON
a) Tính chất hấp phụ
Than gỗ, than xương có tính hấp phụ (giữ trên bề mặt của chúng các chất khí, chất hơi, chất tan trong dung dịch). Nhờ tính chất này mà những than gỗ, than xương có tính hấp phụ cao (gọi là than hoạt tính) được dùng để làm trắng đường, chế tạo mặt nạ phòng độcr..
b) Tính chất hóa học
Tính chất hóa học đặc trưng của cacbon là tính khử, nhiệt độ càng cao tính khử của cacbon càng mạnh.
- Tác dụng với oxi
C + O2 \[\overset{{{t}^{0}}}{\mathop{\to }}\,\] CO2
- Tác dụng với một sô oxit kim loại ở nhiệt độ cao như CuO, PbO,…
C + 2CuO \[\overset{{{t}^{0}}}{\mathop{\to }}\,\] 2Cu + CO2
- Tác dụng với hơi nước ở nhiệt độ cao
C (nóng đỏ) + H2O (hơi)\[\overset{{{t}^{0}}}{\mathop{\to }}\,\] CO + H2
Hỗn hợp {CO, H2} gọi là khí than ướt, được dùng làm nhiên liệu khí.
IV. TỔNG KẾT
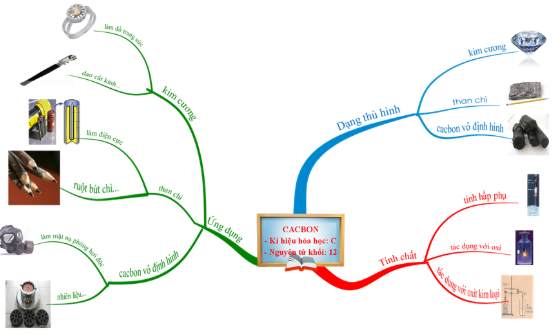
Bài tập minh họa
Bài 1. Dẫn khí CO dư qua ống đựng bột một oxit sắt (FexOy) ở nhiệt độ cao. Sau khi phản ứng kết thúcthu được 0,84 gam sắt và dẫn khí sinh ra vào nước vôi trong dư thì thu được 2 gam kết tủa. Xác định công thức phân tử của FexOy.
Hướng dẫn
nCaCO3 = \[\frac{2}{100}\]= 0,02 mol; nFe = \[\frac{0,81}{56}\]= 0,015 mol
Phản ứng : FexOy + yCO ----> xFe + yCO2
\[\frac{0,02x}{y}\] 0,02
CO2 + Ca(OH)2 ------> CaCO3 + H2O
0,02 0,02
Ta cso nFe =\[\frac{0,02x}{y}\] = 0,015 => \[\frac{0,015}{0,02}=\frac{3}{4}\]
Vậy CTPT của oxit là Fe2O3
Bài 2. Khử 16 gam hỗn hợp các oxit kim loại : FeO, Fe2O3, Fe3O4, CuO và PbO bằng khí CO ở nhiệt độ cao, khối lượng chất rắn thu được là 11,2 gam. Tính thể tích khí CO đã tham gia phản ứng (đktc).
Hướng dẫn
áp dung ĐLBT khối lượng
nCO2 = nCO = x mol
moxit + mCO = mchất rắn +mCO2
28x – 44x = 11,2 – 16 => x = 0,3.
Vậy VCO = 0,3.22,4 = 6,72 lit
B. BÀI TẬP VÀ HƯỚNG DẪN GIẢI
Câu 1. (Trang 84 SGK)
Dạng thù hình của nguyên tố là gì ? Cho hai thí dụ.
Hướng dẫn giải
Khí niệm về dạng thù hình: Dạng thù hình của nguyên tố là những đơn chất khác nhau do cùng một nguyên tố hóa học tạo nên.
Một nguyên tố hóa học có thể tạo ra hai hay nhiều đơn chất.
- cacbon có 3 dạng thù hình: kim cương, than chì , cacbon vô định hình.
- oxi có 2 dạng thù hình là: khí oxi và ozon.
Câu 2. (Trang 84 SGK)
Viết phương trình hoá học của cacbon với các oxit sau:
a) CuO ;
b) PbO ;
c) CO2;
d) FeO.
Hãy cho biết loại phản ứng ; vai trò của C trong các phản ứng ; ứng dụng của các phản ứng đó trong sản xuất.
Hướng dẫn giải
a) С + 2CuO \[\overset{{{t}^{0}}}{\mathop{\to }}\,\]2Cu + CO2
=>Đây là phản ứng oxi hóa khử, C đóng vai trò làm chất khử, phản ứng này dùng để điều chế kim loại đồng.
b) С + 2PbO \[\overset{{{t}^{0}}}{\mathop{\to }}\,\]2Pb + CO2
=>Đây là phản ứng oxi hóa khử, C đóng vai trò làm chất khử, phản ứng này dùng để điều chế kim loại chì
c) С + CO2 \[\overset{{{t}^{0}}}{\mathop{\to }}\,\]2CO
=>Đây là phản ứng oxi hóa khử, C đóng vai trò làm chất khử, phản ứng xảy ra trong quá trình luyện gang.
d) С + 2FeO \[\overset{{{t}^{0}}}{\mathop{\to }}\,\]2Fe + CO2
=>Đây là phản ứng oxi hóa khử, C đóng vai trò làm chất khử, phản ứng xảy ra trong quá trình luyện gang.
Câu 3. (Trang 84 SGK)
Hãy xác định công thức hoá học thích hợp của A, B, C, D trong thí nghiệm ở hình vẽ 3.10. Nêu hiện tượng thí nghiệm và viết phương trình hoá học.
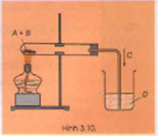
Hướng dẫn giải
Hiện tượng: ta thấy chất rắn màu đen dần chuyển thành chất rắn màu đỏ phần ống nghiệp sát với ngọn lửa đèn cồn, nước vôi trong bị vẩn đục dần.
=>A là CuO, B là C (cacbon), C là khí CO2, D là dung dịch Ca(OH)2
C(r) + 2CuO(r) \[\overset{{{t}^{0}}}{\mathop{\to }}\,\] CO2(k) + 2Cu(r)
CO2 + Ca(OH)2 → CaCO3 + H2O
Câu 4. (Trang 84 SGK)
Tại sao sử dụng than để đun nấu, nung gạch ngói, nung vôi lại gây ô nhiễm môi trường. Hãy nêu biện pháp chống ô nhiễm môi trường và giải thích.
Hướng dẫn giải
Trong than có chứa cả lưu huỳnh và khi nung C phản ứng không hoàn toàn vì vậy khi sử dụng than để đun nấu, nung gạch ngói, nung vôi sẽ sinh ra CO2, CO, SO2 . Những khí này đều ảnh hưởng không tốt đến thực, động vật, con người, gây ra mưa axit, hiệu ứng nhà kính, ...
Để giảm thiểu những tác hại đó nên xây lò nung vôi, gạch ngói ở nơi xa dân cư, đông thời trông cây xanh đế hấp thụ khí CO2 và giải phóng khí oxi.
Câu 5. (Trang 84 SGK)
Trong công nghiệp, người ta sử dụng cacbon để làm nhiên liệu. Tính nhiệt lượng toả ra khi đốt cháy 5 kg than chứa 90% cacbon, biết 1 mol cacbon cháy toả ra 394 kJ.
Hướng dẫn giải
Trong 5 kg than có: mC = 5.90% = 4,5 kg = 4500 gam
=>nC = \[\frac{4500}{12}\](mol)
Nhiệt lượng tỏa ra khi đốt cháy 5kg than là:
Q = nC . 394 = 147750 (kJ)
C. BÀI TẬP TRẮC NGHIỆM
Câu 1: Chất dùng làm chất khử một số kim loại ở nhiệt độ cao là:
A. Oxi
B. Cacbon
C. Photpho
D. Lưu huỳnh
Câu 2: Để khẳng định một chất bột là cacbon hay oxit sắt , cách làm nào sau đây là đúng? A. Cho mỗi loại vào muỗng sắt đun trên ngọn lửa đèn cồn
B. Cho mỗi loại tác dụng với H2 ở nhiệt độ cao.
C. Đun nóng mỗi loại bột trong chén sứ
D. Cả 3 cách đều đúng
Đáp án 1B,2D.







