Lý thuyết về Este
I. Khái niệm
- Este là sản phẩm được tạo thành khi nhóm –OH ở gốc cacboxyl của acid cacboxylic được thay bằng nhóm –OR’ của ancol.
- Công thức của 1 số este thường gặp:
+) Este tạo bởi acid đơn chức R-COOH và ancol đơn chức R’-OH: R-COO-R’
+) Este tạo bởi acid no đơn chức và ancol no đơn chức: CnH2nO2 ( n>=2 )
+) Este tạo bởi acid đa chức R-(COOH)n và ancol đơn chức: R-(COO-R’)n
+) Este tạo bởi acid đơn chức R-COOH và ancol đa chức R’-(OH)n: (R-COO)n-R’
+) Este tạo bởi acid đa chức R-(COOH)n và ancol đa chức R'-(OH)m: Rm(COOR’)n.mR’n
- Đồng phân: Ta có công thức tính nhanh số đồng phân của este no đơn chức (không nên nhớ máy móc):
Số este của CnH2nO2 = 2n-2 (n < 5)
Ví dụ: Số đồng phân este ứng với công thức phân tử C4H8O2 là: 24-2 = 4
Đồng phân este đơn chức gồm có: đồng phân mạch cacbon của gốc acid tạo thành este và đồng phân mạch cacbon của gốc ancol.
Ví dụ: C4H8O2 có các đồng phân este sau:
HCOOCH2-CH2-CH3: n-propyl fomat
CH3COOC2H5: etyl axetat
HCOOCH-(CH3)2: isopropyl fomat
C2H5COOCH3: metyl propionat
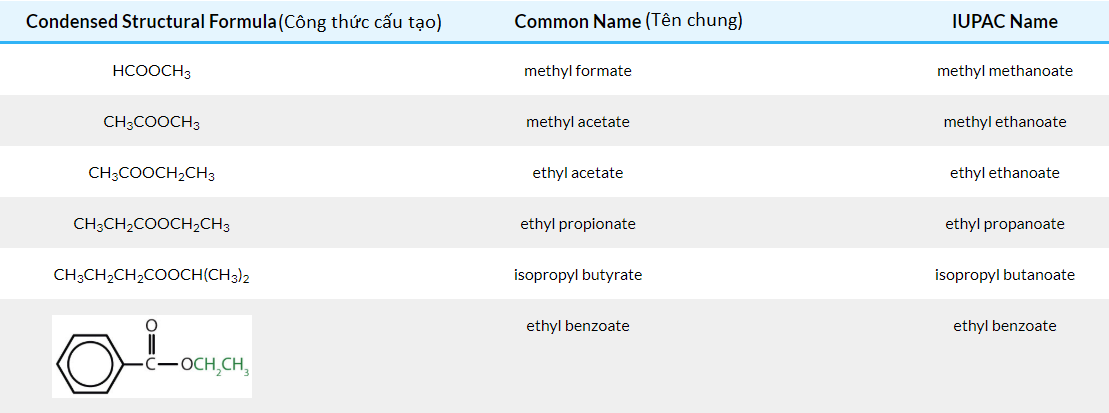
II. Danh pháp
1. Ancol đơn chức: Tên este = tên gốc hydrocacbon R’+ tên gốc acid (đổi đuôi "ic" thành "at" )
Ví dụ:
CH3-COO-CH3: metyl axetat
CH2=CH-COO-CH3: metyl acrylat
2. Với ancol đa chức: Tên este = tên ancol + tên gốc acid
III. Tính chất
- Este có phản ứng xà phòng hoá và phản ứng thủy phân
- Đa số ở trạng thái lỏng. Những este có Phân tử khối rất lớn có thể ở trạng thái rắn (như mỡ động vật, sáp ong …).
- Có nhiệt độ sôi thấp, dễ bay hơi do không tạo liên kết hidro giữa các phân tử.
- Ít tan hoặc không tan trong nước do không tạo liên kết hidro giữa các phân tử với nước.
- Có mùi thơm đặc trưng:
+) CH3COOC10H17: Geranyl axetat: mùi hoa hồng
+) CH3COO(CH2)2CH(CH3)2: Isopentyl acetat: mùi chuối
+) CH3CH2CH2COOC2H5: Etyl butirat và C2H5COOC2H5: etyl propionat: mùi dứa
IV. Tính chất Hóa học của Este

Written by: Long Lengoc - Vietnam National University







