A – TÓM TẮT KIẾN THỨC
I. Khái niệm , danh pháp, cấu tạo phân tử
1. Khái niệm
- Amino axit là loại hợp chất hữu cơ tạp chức mà phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl (COOH).
- Công thức chung của amino axit: (NH2)x R (COOH)y.
2. Danh pháp
- Có thể coi amino axit là axit cacboxylic có nhóm thế amino.
Tên thay thế: axit + số chỉ vị trí nhóm NH2 + amino+ tên mạch chính + oic
- Tên bán hệ thống: axit + kí hiệu chỉ vị trí nhóm NH2 + amino+ tên thông thường của axit tương ứng.
Chú ý: kí hiệu chỉ vị trí:
C – C – C – C – C – C – COOH
ω ε δ γ β α
3. Cấu tạo phân tử
- Ở trạng thái kết tinh amino axit tồn tại ở dạng ion lưỡng cực.
H2N – CH2 – COOH \[\rightleftarrows \] H3N+ - CH2 – COO -
Dạng phân tử dạng ion lưỡng cực
II. Tính chất hóa học.
1. Tính lưỡng tính
- Amino axit tác dụng với dd axit vô cơ mạnh và dd bazơ mạnh.
H2NCH2COOH + HCl → ClH3NCH2COOH
H2NCH2COOH + NaOH → H2NCH2COONa + H2O
2. Tính chất axit – bazơ của dung dịch amino axit.
- Amino axit (NH2)x R (COOH)y
- Khi x = y, pHdd ≈ 7
- Khi x > y, pHdd > 7
- Khi x < y, pHdd < 7
3. Phản ứng este hóa nhóm COOH.
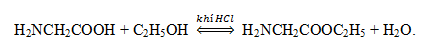
4. Phản ứng trùng ngưng.
- Các amino axit có nhóm NH2 từ C6 trở lên tham gia phản ứng trùng ngưng khi có xúc tác, nhiệt độ tạo polime thuộc loại poliamit.
H2N[CH2]5COOH \[\overset{xt,{{t}^{0}}}{\mathop{\to }}\,\] (- NH[CH2]5COO -)n + H2O
Tơ nilon - 6
- OH của nhóm COOH ở phân tử amino axit này kết hợp với H của nhóm NH2 kia tạo thành phân tử nước H2O.
IV. Ứng dụng
- Amino axit thiên nhiên (hầu hết α – amino axit) là cơ sở để kiến tạo nên các loại protein của cơ thể sống. Protein có vai trò là nền tảng về cấu trúc và chức năng của mọi cơ thể sống.
- Bột ngọt là muối mononatri của axit glutamic. Axit glutamic là thuốc hỗ trợ thần kinh.
- Axit – 6 – amino hexanoix và axit – 7 – amino heptanoic là nguyên liệu để sản xuất tơ nilon – 6, nilon – 7.
B – GIẢI BÀI TẬP SÁCH GIÁO KHOA
Câu 1.(Trang 48/SGK)
Ứng với công thức phân tử C4H9NO2 có bao nhiêu amino axit đồng phân cấu tạo của nhau ?
A. 3.
B. 4.
C. 5.
D. 6.
Bài làm:
Đáp án C
Nhóm NH2 vị trí γ
H2N – CH2 – CH2– CH2 – COOH
=>Tương tự nhóm NH2 ở vị trí β, α
H2N – CH2 – CH(CH3)COOH
CH3 – C(NH2)(CH3)COOH
Câu 2.(Trang 48/SGK)
Có ba chất hữu cơ: H2NCH2COOH, CH3CH2COOH và CH3[CH2]3NH2.
Để nhận ra dung dịch của các hợp chất trên, chỉ cẩn dùng thuốc thử nào sau đây ?
A. NaOH.
B. HCl.
C. CH3OH/HCl.
D. Quỳ tím.
Bài làm:
Đáp án D
Nhỏ vài giọt mẫu chất vào quỳ tím
Mẫu làm quỳ tím chuyển đỏ: CH3CH2COOH
Mẫu làm quỳ tím chuyển xanh: CH3[CH2]3NH2
Mẫu làm quỳ tím không chuyển màu:H2NCH2COOH
Câu 3.(Trang 48/SGK)
α-Amino axit X có phần trăm khối lượng các nguyên tố C, H, N lần lượt bằng 40,45%, 7,86%, 15,73%, còn lại là oxi và có công thức phân tử trùng với công thức đơn giản nhất. Xác định công thức cấu tạo và gọi tên của X.
Bài làm:
Gọi CTPT của X là CxHyOzNt
Ta có % khối lượng của O trong X là
%mO = 100% – (%mC + %mH + %mN) = 35,96%
=>%mC : %mH : %mO : %mN = x : y : z : t = \[\frac{40,45}{12}:\frac{7,86}{1}:\frac{15,73}{14}:\frac{35,96}{16}=3:7:1:2\]
CTĐG của X là C3H7NO2 => CTPT: C3H7NO2
CTCT của X là: H2N-CH(CH3)-COOH: alanin.
Câu 4.(Trang 48/SGK)
Viết phương trình hóa học của các phản ứng giữa axit 2-aminopropanoic với:
NaOH; H2SO4; CH3OH có mặt khí HCl bão hòa.
Bài làm:
Axit 2-aminopropanoic phản ứng với NaOH; H2SO4; CH3OH có mặt khí HCl bão hòa.
CH3 – CH(NH2)COOH + NaOH → CH3 – CH(NH2)COONa + H2O.
2CH3 – CH(NH2)COOH + H2SO4 → [CH3 – CH(NH3)COOH]SO4
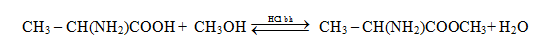
Câu 5.(Trang 48/SGK)
Viết phương trình hóa học của phản ứng trùng ngưng các amino axit sau:
a) Axit 7-aminoheptanoic;
b) Axit 10-aminođecanoic.
Bài làm:
a) 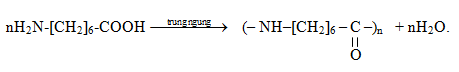
b)
Câu 6.(Trang 48/SGK)
Este A được điều chế từ amino axit B (chỉ chứa C, H, N, O) và ancol metylic. Tỉ khối hơi của A so với H2 là 44,5. Đốt cháy hoàn toàn 8,9 gam este A thu được 13,2 gam CO2, 6,3 gam H2O và 1,12 lít N2 (đo ở đktc).
Xác định công thức, viết công thức cấu tạo của A và B.
Bài làm:
A tỉ khối so với H2 là 44,5 => MA = 44,5 . 2 = 89 (g/mol)
Ta có: mC = \[\frac{13,2.12}{44}=3,6\](gam);
mH = \[\frac{6,3.2}{18}=0,7\] (gam)
mN = \[\frac{11,2.28}{22,4}=1,4\] (gam);
mO = 8,9 – (3,6 + 0,7 + 1,4) = 3,2 (gam)
Gọi CTPT của A là CxHyOzNt,
=> mC : mH : mO : mN = x : y : z : t = \[\frac{3,6}{12}:\frac{0,7}{1}:\frac{3,2}{16}:\frac{1,4}{14}=0,3:0,7:0,2:0,1=3:7:2:1\]=> CTĐG của A là (C3H7O2N)n ; MA = 89 g/mol => n = 1
Vậy CTPT của A là C3H7O2N
CTCT: H2N-CH2-COOCH3 (A) ; H2N-CH2-COOH (B).
C – BÀI TẬP NÂNG CAO
Bài 1:
Cho 13,23 gam axit glutamic phản ứng với 200 ml dung dịch HCl 1M thu được dung dịch X. Cho 400 ml dung dịch NaOH 1M vào X được Y. Cô cạn Y thu được m gam rắn khan, biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Hướng dẫn:
Axit glutamic có dạng: HOOC – CH2 – CH2 – CH(NH2) – COOH
⇒ naxit glutamic = 0,09 mol
Có nHCl = 0,2 mol; nNaOH = 0,4 mol
⇒ nNaOH dư = nNaOH ban đầu – (2nGlutamic + nHCl) = 0,02 mol
⇒ Chất rắn khan gồm:
0,02 mol NaOH;
0,09 mol NaOOC – CH2 – CH2 – CH(NH2) – COONa;
0,2 mol NaCl.
⇒ m = 29,69 g
Bài 2:
Cho 4,41 gam một amino axit X tác dụng với dung dịch NaOH dư cho ra 5,73 gam muối. Mặt khác cũng lượng X như trên nếu cho tác dụng với dung dịch HCl dư thu được 5,505 g muối clorua. Công thức cấu tạo của X là:
Hướng dẫn:
Cứ 1 gốc -COOH + NaOH 1 gốc -COONa
và 1 gốc -NH2 + HCl 1 gốc -NH3Cl
\(\Rightarrow\) Khi X + NaOH dư:
\(\Rightarrow \Delta m = m _{muoi} - m_X = m_{COONa} - m_{-COOH}\)
\(\Rightarrow n_{-COOH}\times (67 - 45) = 5,73 - 4,41\)
\(\Rightarrow n_{-COOH} = 0,06\ (mol)\)
Khi X + HCl ta có:\(\Delta m = m_{muoi} - m_X = m_{-NH_3Cl} - m_{-NH_2}\)
\(\Rightarrow n_{-NH_2}\times (52,5 - 16) = 5,505 - 4,41\)
\(\Rightarrow n_{-NH_2} = 0,03\ (mol)\)
\(\Rightarrow\) Ta thấy trong 4,41 g X có
\(\left\{\begin{matrix} 0,03 \ mol-NH_2\\ 0,06 \ mol-COOH \end{matrix}\right.\)
\(\Rightarrow\) Đặt CTPT X là: R(COOH)2n(NH2)n \(\Rightarrow\) nX = (mol)
\(\Rightarrow\) MX = R + 90n + 16n
⇔ R = 41n
Ta thấy: n = 1; MR = 41 \(\Rightarrow\) R = C3H5 thỏa mãn
\(\Rightarrow\) X là HOOC-CH2-CH(NH2)-CH2-COOH hoặc HOOC-CH(NH2)-CH2-CH2-COOH







