I. Định nghĩa
Định nghĩa: Phenol là những HCHC trong phân tử có nhóm OH liên kết trực tiếp với nguyên tử cacbon của vòng benzen.
II. Phenol
Tính chất hoá học
- Nhân hút e, –OH đẩy e
a. Phản ứng thế nguyên tử hiđro của nhóm OH
* Tác dụng với kim loại kiềm: C6H5OH + Na → C6H5ONa + H2
* Tác dụng với bazơ: C6H5OH + NaOH → C6H5ONa + H2O
→ Phenol có tính axit, tính axit của phenol rất yếu; dung dịch phenol không làm đổi màu quỳ tím.
Chú ý: tính axit yếu, không làm đổi màu quỳ tím, thứ tự: nấc II của H2CO3 < phenol < nấc I của H2CO3
=> Có phản ứng
C6H5ONa + H2O + CO2 → C6H5OH + NaHCO3
C6H5OH + Na2CO3 →C6H5ONa + NaHCO3
b. Phản ứng thế nguyên tử hiđro của vòng benzen:
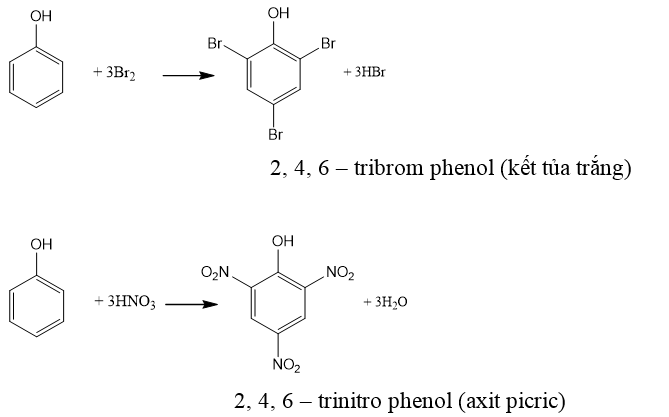
4. Điều chế
Theo 2 cách:
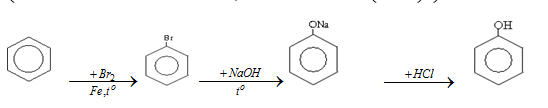
Cách 1: Nhựa than đá →chưng cất→ C6H6 +Cl2(xt Fe)→ C6H5Cl
+ NaOH (tocao, p cao)→ C6H5ONa + CO2+H2O→ C6H5OH
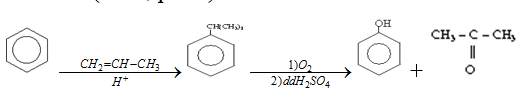
Cách 2: Từ cumen (iso propylbenzen)
C6H5CH(CH3)2 ----1)O2(kk):2)H2SO4→ C6H5OH + CH3COCH3
(C6H6 ----CH2=CH-CH3, to → C6H5CH(CH3)2)
Bài 1 (Trang 193 – SGK)
.png)
Lời giải

Bài 2 (Trang 193 – SGK)
Từ benzen và các chất vô cơ cần thiết có thể điều chế được các chất sau:
2,4,6-tribomphenol (1) ; 2,4,6-trinitrophenol (2)
Viết phương trình hóa học của các phản ứng xảy ra.
Lời giải

Giải thích
a) Sai vì theo định nghĩa ancol thơm: phân tử có nhóm –OH liên kết với nguyên tử C no thuộc mạch nhánh của vòng benzen. VD: C6H5CH2OH
d) Sai vì tính axit của dung dịch phenol rất yếu, không làm đổi màu quỳ tím.
Bài 3 (Trang 193 – SGK)
Cho 14,0 gam hỗn hợp A gồm phenol và etanol tác dụng với natri dư thu được 2,24 lít khí hidro (đktc)
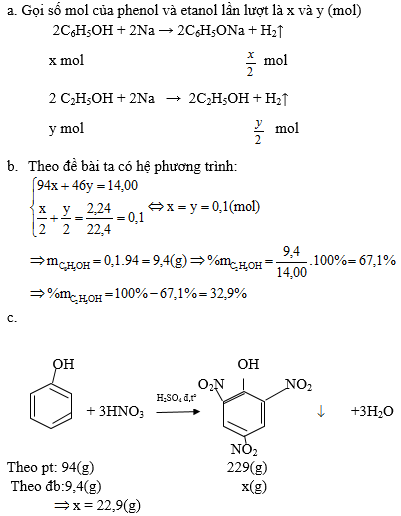
a. Viết các phương trình hóa học xảy ra.
b. Tính thành phần phần trăm khối lượng của mỗi chất trong A.
c. Cho 14,0 gam hỗn hợp A tác dụng với HNO3 thì thu được bao nhiêu gam axit picric (2,4,6- trinitrophenol)?
Lời giải
Bài 4 (Trang 193 – SGk)
Cho từ từ phenol vào nước brom; stiren vào dung dịch brom trong CCl4. Nêu hiện tượng và viết các phương trình hóa học.
Lời giải
.png)
Bài 5 (Trang 193 – SGK)
Sục khí CO2 vào dung dịch natri phenolat thấy dung dịch vẩn đục, trong dung dịch có NaHCO3 được tạo thành. Viết phương trình hóa học của phản ứng xảy ra và giải thích. Nhận xét về tính axit của phenol.
Lời giải
\[{{C}_{6}}{{H}_{5}}ONa+C{{O}_{2}}+{{H}_{2}}O\xrightarrow{{{t}^{0}}}{{C}_{6}}{{H}_{5}}OH\downarrow +NaHC{{O}_{3}}\]
- Dung dịch bị vẩn đục là do phản ứng tạo ra phenol.
- Nhận xét về tính axit của phenol: Phenol có tính axit yếu hơn nấc thứ nhất của axit cacbonic H2CO3, nên bị axit cacbonic đẩy ra khỏi dung dịch muối.
Bài 6 (Trang 193 – SGk)
Viết các phương trình hóa học điều chế:
- phenol từ benzen (1)
- stiren từ etylbenzen (2)
Các chất vô cơ cần thiết coi như có đủ.
Lời giải
- (1) Điều chế phenol phenol từ benzen:
C6H6 + Br2 ---Fe, to→ C6H5Br + HBr
C6H5Br + 2NaOHđặc ---to cao, P cao→ C6H5ONa + NaBr + H2O
C6H5ONa + CO2 + H2O ---to→ C6H5OH + NaHCO3
- (2) Điều chế stiren từ etybenzen:
.png)







