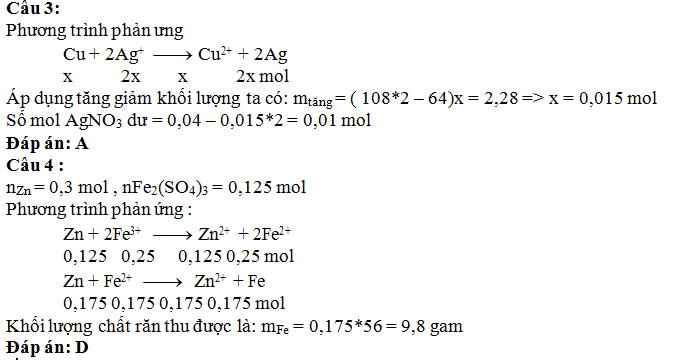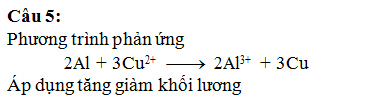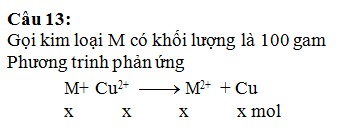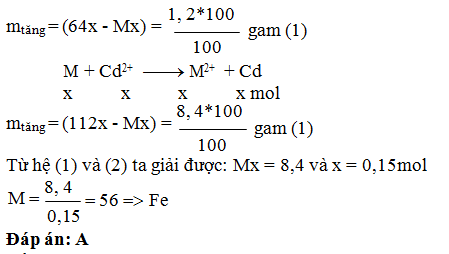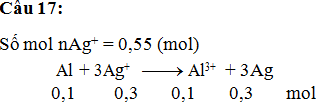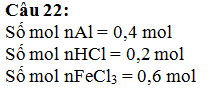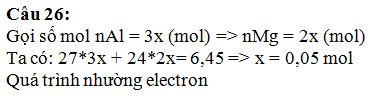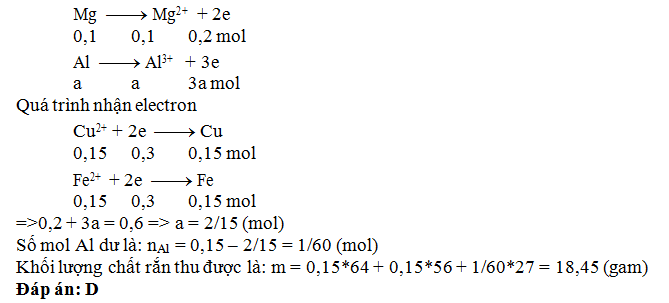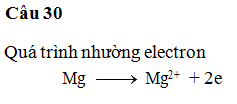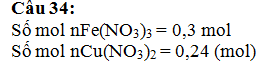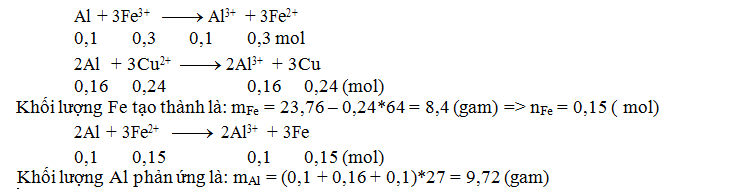Kim loại tác dụng với dung dịch muối
Phần 1 . Lý thuyết:
A + muối của kim loại B -> muối của kim
loại A + B
Điều
kiện :
- - Muối của B phải tan.
- - A không tác dụng với H2O ở điều kiện thường
- - A có tính khử > B
-Kim loại B sinh ra thường bám vào kim loại
A ban đầu làm cho thanh kim loại ban đầu có khối lượng tăng lên hoặc giảm đi.
mthanh kim loại thay đổi = m dd
muối thay đổi.
mKL tăng = mKL sinh ra –
mKL pư => % m kim loại tăng = 
mKL
giảm = mKL phản ứng – m kim loại
sinh ra => %m kim loại giảm = 
- -Khi cho kim loại tác dụng với dung dịch chứa nhiều muối thì phản ứng xảy
ra theo thứ tự: muối của kim loại yếu hơn pư trước -> vì vậy thứ tự xuất hiện
kim loại trong chất rắn thu được là từ kim loại yếu nhất của bài toán ngược lên
trên dãy điện hóa.
- -Khi cho hỗn hợp kim loại vào dung dịch chứa 1 muối thì phản ứng xảy ra
theo thứ tự kim loại mạnh hơn phản ứng trước.
è
Thứ tự xuất hiện muối trong dung dịch thu được là từ muối của kim loại mạnh
nhất ngược xuống dãy điện hóa.
- - Dung dịch muối Fe3+ phản
ứng với kim loại từ Mg -> Cu tạo ra muối Fe2+
VD. nếu cho Al hoặc Zn hoặc Mg vào dung dịch
Fe3+:
Phản ứng theo thứ tự :
kim loại + Fe3+ -> Fe2+
kim loại dư+ Fe2+ -> Fe
- -Dung dịch muối Fe2+ có tính khử như 1 kim loại, phản ứng được
với muối Ag -> dd Fe3+
+ Nếu cho Fe vào dung dịch AgNO3
Pư
theo thứ tự: Fe + 2AgNO3 -> Fe(NO3)2 + 2Ag
Fe(NO3)2
+ AgNO3 -> Fe(NO3)2 + Ag
+
FeCl2 + 3AgNO3 -> Fe(NO3)3 + 2
AgCl + Ag
FeBr3
Phần 2. Bài tập mẫu:
VD1. Cho hỗn hợp gồm Al và Zn vào dung dịch
AgNO3. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch X chỉ
chứa một muối và phần không tan Y gồm hai kim loại. Hai kim loại trong Y và muối trong X là:
A.
Al, Ag và Zn(NO3)2
B.
Al, Ag và Al(NO3)3
C.
Zn , Ag và Al(NO3)3
D.
Zn, Ag và Zn(NO3)2
Hướng dẫn giải:
Hai kim loại trong Y là hai kim loại có
tính khử yếu nhất là Ag và Zn
Al + 3Ag+ -> Al3+
+ 3Ag
Muối thu được là muối cả kim loại có tính
khử mạnh nhất
ð
Muối X là Al(NO3)3
=> đáp án C
VD2. Cho 2,24 gam bột sắt vào 200ml dung dịch chứa hỗn hợp gồm AgNO3
0,1M và Cu(NO3)2 0,5M. sau khi các phản ứng xảy ra hoàn
toàn thu được dung dịch X và m gam chất rắn Y. giá trị của m là:
A.
2,80
B.
2,16
C.
4,08
D. 0,64

Phần 3. Bài tập vận dụng:
Câu 1: Nhúng một tấm Fe có khối lượng 10
gam vào dung dịch CuCl2, sau một thời gian phản ứng khối lượng tấm
kim loại tăng lên so với ban đầu là 0,75 gam. Hàm lượng Fe trong tấm sắt sau
phản ứng là
A. 100%. B. 44,18%. C. 95,09%. D. 62,5%.
Câu 2: Hoà tan 25 gam muối CuSO4.5H2O
vào nước được 500 ml dung dịch. Cho dần mạt sắt vào 50 ml dung dịch trên, khuấy
nhẹ cho đến khi hết màu xanh. Khối lượng chất rắn thu được sau phản ứng tăng
hay giảm bao nhiêu gam?
A. Tăng 0,8 gam.
B. Tăng 0,08 gam.
C. Giảm 0,08 gam.
D.
Giảm 0,8 gam.
Câu 3: Ngâm một thanh Cu trong dung dịch
có chứa 0,04 mol AgNO3, sau một thời gian lấy thanh kim loại ra thấy
khối lượng tăng hơn so với lúc đầu là 2,28 gam. Coi toàn bộ kim loại sinh ra
đều bám hết vào thanh Cu. Số mol AgNO3 còn lại trong dung dịch là
A. 0,01. B. 0,005. C. 0,02. D. 0,015.
Câu 4: Hoà tan 19,5 gam Zn vào 250 ml
dung dịch chứa Fe2(SO4)3 0,5M. Sau khi phản
ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 8,4 gam. B. 11,375 gam. C. 11,2
gam. D. 9,8 gam.
Câu 5: Nhúng một thanh Al nặng 50 gam vào
400 ml dung dịch CuSO4 0,5M. Sau một thời gian phản ứng lấy thanh Al
ra cân nặng 51,38 gam. Khối lượng Cu thoát ra và nồng độ của muối nhôm có trong
dung dịch (coi V không đổi) là:
A. 1,92 gam
và 0,05M. B. 2,16 gam và 0,025M.
C. 1,92 gam
và 0,025M. D. 2,16 gam và 0,05M.
Câu 6: Nhúng một thanh graphit phủ một
kim loại A hóa trị II vào dung dịch CuSO4 dư. Sau phản ứng, thanh
graphit giảm 0,04 gam. Tiếp tục nhúng thanh này vào dung dịch AgNO3
dư tới khi phản ứng kết thúc thì khối lượng tăng 6,08 gam (so với sau khi nhúng
vào CuSO4). Kim loại A là
A. Ca. B. Cd. C. Zn. D. Cu.
Câu 7: Nhúng một thanh Al nặng 20 gam vào
400 ml dung dịch CuCl2 0,5M. Khi nồng độ dung dịch CuCl2
giảm 25% thì lấy thanh Al ra khỏi dung dịch, giả sử tất cả Cu thoát ra bám vào
thanh Al. Khối lượng thanh Al sau phản
ứng là
A. 21,15
gam. B. 21,88 gam. C. 22,02
gam. D. 22,3 gam.
Câu 8: Ngâm một vật bằng Cu có khối lượng 10 gam trong 250 ml dung dịch
AgNO3 4%.
Khi lấy
vật ra khỏi dung dịch thì
khối lượng AgNO3
trong dung dịch giảm 17%. Khối lượng của vật sau phản ứng là
A. 27 gam. B. 10,76
gam. C. 11,08 gam. D. 17
gam.
Câu 9: Nhúng thanh kim loại M hoá trị II vào dung
dịch CuSO4,
sau một thời gian lấy thanh kim loại ra thấy khối lượng giảm 0,05%. Mặt khác,
nhúng thanh kim loại trên vào dung dịch Pb(NO3)2, sau một thời gian thấy khối lượng tăng 7,1%. Biết rằng số mol của CuSO4 và Pb(NO3)2 tham
gia ở 2 trường hợp là như nhau. Kim loại
M đó là
A. Mg. B. Al. C. Fe. D. Zn.
Câu 10: Cho hai thanh kim loại R (hóa trị
II) có cùng khối lượng. Nhúng thanh thứ nhất vào dung dịch Cu(NO3)2
và thanh thứ hai vào dung dịch Pb(NO3)2. Sau một thời
gian khi số mol hai muối bằng nhau, lấy hai thanh kim loại đó ra khỏi dung dịch
thấy khối lượng thanh thứ nhất giảm 0,2% còn khối lượng thanh thứ hai tăng
28,4% . Nguyên tố R là
A. Mg. B. Cu. C. Fe. D. Zn.
Câu 11.
: Có 2 lá kim loại cùng chất, cùng khối
lượng, có khả năng tạo ra hợp chất có số oxi hoá +2. Một lá được ngâm trong
dung dich Pb(NO3)2 và lá kia được ngâm trong dung dịch
Cu(NO3)2. Sau 1 thời gian người ta lấy các lá kim loại ra
khỏi dung dịch, rửa nhẹ, làm khô. Nhận thấy khối lượng lá kim loại ngâm trong
muối chì tăng 19%, còn lá kim loại kia giảm 9,6%. Biết rằng, trong 2 phản ứng
trên, khối lượng các kim loại bị hoà tan như nhau. Lá kim loại đã dùng là
A. Mg. B. Zn. C. Cd. D. Fe.
Câu 12: Một thanh kim loại M hoá trị II
nhúng vào 2 lít dung dịch FeSO4, sau phản ứng khối lượng thanh kim
loại M tăng 32 gam. Cũng thanh kim loại ấy nhúng vào 2 lít dung dịch CuSO4,
sau phản ứng khối lượng thanh M tăng 40 gam (giả sử toàn bộ lượng kim loại
thoát ra đều bám lên thanh kim loại M và các phản ứng xảy ra hoàn toàn). Kim
loại M đã dùng và nồng độ mol của dung dịch CuSO4 là:
A. Zn; 0,4M. B. Cd; 0,6M. C. Mg;
0,5M. D. Ba; 0,7M.
Câu 13: Lấy 2 thanh kim loại cùng khối
lượng cùng một kim loại M hóa trị 2. Thanh 1 nhúng vào dung dịch CuCl2;
thanh 2 vào dung dịch CdCl2, hai dung dịch này có cùng thể tích và
cùng nồng độ mol. Sau một thời gian, thanh 1 có khối lượng tăng 1,2%; thanh 2
tăng 8,4%. Số mol muối trong 2 dung dịch giảm như nhau. Kim loại M là:
A. Zn. B. Fe. C. Mg. D. Ni.
Câu 14: Cho 12,8 gam kim loại X hóa trị II
phản ứng hoàn toàn với khí Cl2 thu được muối Y. Hòa tan muối Y vào
nước để được 400 ml dung dịch Z. Nhúng thanh Zn nặng 13,0 gam vào Z, sau một
thời gian thấy kim loại X bám vào thanh Zn và khối lượng thanh Zn lúc này là
12,9 gam, nồng độ ZnCl2 trong dung dịch là 0,25 M. Kim loại X và
nồng độ mol của muối Y trong dung dịch Z lần lượt là:
A. Cu; 0,5M. B. Fe; 0,57M. C. Cu; 0,25M. D. Fe; 0,25M.
Câu 15: Hai thanh kim loại X cùng chất,
đều có khối lượng là a gam.Thanh thứ nhất nhúng vào 100 ml dung dịch AgNO3;
thanh thứ 2 nhúng vào 1,51 lít dung dịch Cu(NO3)2. Sau 1
thời gian lấy 2 thanh kim loại ta thấy
thanh 1 tăng khối lượng, thanh 2 giảm khối lượng nhưng tổng khối lượng 2 thanh
vẫn là 2a gam, đồng thời trong dung dịch thấy nồng độ mol của muối kim loại X
trong dung dịch Cu(NO3)2 gấp 10 lần trong dung dịch AgNO3.
Kim loại X là (biết rằng X có hóa trị II)
A. Cd. B. Zn. C. Pb. D. Fe.
Câu 16: Hỗn hợp X gồm 2,7 gam Al và 5,6
gam Fe. Cho X vào 200 ml dung dịch AgNO3 1,75M. Sau khi phản ứng
hoàn toàn thu được dung dịch Y. Khối lượng chất rắn sau phản ứng là
A. 38 gam B. 40 gam C. 42
gam D. 44 gam
Câu 17:Cho hỗn hợp bột gồm 2,7 gam Al và
5,6 gam Fe vào 550 ml dung dịch AgNO3 1M. Sau khi các phản ứng xảy
ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là
A. 32,4. B. 64,8. C. 59,4. D. 54,0.
(Trích đề thi tuyển
sinh ĐH – CĐ khối A – 2008)
Câu 18: Cho 200 ml dung dịch hỗn
hợp hai muối AgNO3 0,1M và Cu(NO3)2 0,5M. Thêm
2,24 gam bột sắt vào dung dịch rồi khuấy đều cho phản ứng hoàn toàn thu được
chất rắn A và dung dịch B. Khối lượng của A là
A. 4,08 gam B. 6,
16 gam C. 7,12 gam D. 8,23 gam
(Trích đề thi tuyển sinh ĐH – CĐ khối B – 2009)
Câu 19: Cho 0,8 mol bột Mg vào dung dịch chứa 0,6 mol FeCl3 và
0,2 mol CuCl2. Sau khi phản ứng kết thúc thu được chất rắn A và dung
dịch B. Cô cạn dung dịch B thì khối lượng chất rắn thu được là
A. 114,1 gam. B. 123,6 gam. C. 143,7
gam. D. 101,2 gam.
Câu 20: Cho 2,24 gam bột Fe vào 100 ml dung dịch hỗn hợp gồm AgNO3
0,1M và Cu(NO3)2 0,5M. Khuấy đều đến khi phản ứng hoàn
toàn thu được chất rắn A và dung dịch B. Khối lượng của chất rắn A là
A. 3,32 gam B. 0,84
gam C. 4,48 gam D.
0,48 gam
Câu 21: Cho 6,48 gam Al tác dụng hoàn toàn với 100 ml dung dịch chứa Fe2(SO4)3
1M và CuSO4 0,8M sau phản ứng thu m gam chất rắn. Giá trị của m là
A. 16,4 gam B. 24,26 gam C. 15,2
gam D. 15,57 gam
Câu 22:Cho 10,8 gam nhôm
vào 500 ml dung dịch chứa HCl 0,4M và FeCl3 1,2M. Sau khi phản ứng
xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 8,4 gam B. 28 gam C. 16,8
gam D. 11,2 gam
Câu 23:
Cho 19,3 gam hỗn hợp bột gồm Zn và Cu có tỉ lệ mol tương ứng là 1
: 2 vào dung dịch chứa 0,2 mol Fe2(SO4)3. Sau
khi các phản ứng xảy ra hoàn toàn thu được m gam kim loại. Giá trị của m là
A. 12 B. 16,53 C. 6,4 D. 12,8
(Trích đề thi tuyển sinh ĐH – CĐ khối A – 2010)
Câu 24:Cho 5,5 gam một hỗn hợp bột Al và
sắt (trong đó số mol Al gấp đôi số mol sắt) vào 300 ml dung dịch AgNO3
1M. Khuấy kĩ cho phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của
m là
A. 32,95 gam B. 35,2
gam C. 39,5 gam D.30,25
gam
Câu 25:Cho 17,6 gam hỗn hợp Fe và Cu có
tỉ lệ mol 2 : 1 vào 416 ml dung dịch AgNO3 1,25M. Sau phản ứng thu
được m (gam) chất rắn A và dung dịch B. Giá trị của m là
A. 32,4 gam B. 60
gam C. 5616
gam D. 58,72 gam
Câu 26: Cho 6,45 gam hỗn hợp bột X gồm hai
kim loại Al và Mg có tỉ lệ tượng ứng là 3:2 vào 150 ml dung dịch Y chứa Fe(NO3)2
1M và Cu(NO3)2 1M, khuấy đều cho đến khi phản ứng kết
thúc thu được m gam chất rắn và dung dịch Z. Giá trị của m là
A. 12,9 B. 21,9 C. 19,2 D. 18,45
Câu 27: Cho 1,1 gam hỗn hợp bột hai kim
loại Al, Fe tác dụng hết với dung dịch H2SO4 đặc, nóng
thu được 1,008 lít SO2 ở đktc. Cũng lượng hỗn hợp này đem hoà tan
vào 100 ml dung dịch AgNO3 0,8M, phản ứng hoàn toàn. Khối lượng chất
rắn tạo ra là
A. 2,45 gam B. 2,84
gam C. 3,24 gam D.
8,64 gam
Câu 28: Cho 0,4 mol Mg vào dung dịch chứa
0,2 mol Cu(NO3)2 và 0,3 mol Fe(NO3)3.
Khối lượng chất rắn thu được sau phản ứng là
A. 11,2 gam. B. 15,6
gam. C. 22,4 gam. D.
12,88 gam.
Câu 29: Trộn hai dung dịch AgNO3
0,42M và Pb(NO3)2 0,36M với thể tích bằng nhau được dung
dịch X. Cho 0,81 gam bột Al vào 100 ml dung dịch X tới phản ứng hoàn toàn được
m gam chất rắn Y. Giá trị của m là
A. 4,851 B. 4,554 C. 6,525 D. 9,054
Câu 30: Hòa tan hỗn hợp chứa 0,1 mol Mg và
0,1 mol Al vào dung dịch hỗn hợp chứa 0,1 mol Cu(NO3)2 và
0,35 mol AgNO3. Khi phản ứng xảy ra hoàn toàn thì khối lượng chất
rắn thu được là
A. 21,6 gam B. 37,8
gam C. 42,6 gam D.
44,2 gam
Câu 31: Cho 0,2 mol Mg và 0,3 mol Al vào
200 ml dung dịch chứa Cu(NO3)2 1M và Fe(NO3)2
1,5M. Sau khi phản ứng xảy ra hoàn toàn ta thu được chất rắn có khối lượng là
A. 29,6 gam B. 32,3
gam C. 33,2 gam D.
12,9 gam
Câu 32: Cho 8,3 gam hỗn hợp X gồm (Al, Fe)
vào 200 ml dung dịch CuSO4 1,05M. Sau khi phản ứng hoàn toàn thu
được 15,68 gam chất rắn Y gồm 2 kim loại. Khối lượng của Fe có trong hỗn hợp X là
A. 2,8 gam B.
4,48gam C. 5,6
gam D. 2,24 gam
Câu 33: Cho hỗn hợp bột gồm 0,15 mol Al và
x mol Mg phản ứng với 500 ml dung dịch FeCl3 0,32M thu được 10,31
gam hỗn hợp 2 kim loại và dung dịch X. Giá trị của x là
A. 0,10 mol. B.
0,12 mol. C. 0,06 mol. D. 0,09 mol.
Câu 34: Cho m gam bột Al vào 400 ml dung
dịch Fe(NO3)3 0,75M và Cu(NO3)2
0,6M sau phản ứng thu được dung dịch X và 23,76 gam hỗn hợp hai kim loại. Giá
trị của m là
A. 9,72 gam. B. 10,8
gam. C. 10,26 gam. D. 11,34
gam.
Câu 35: Cho 1,93 gam hỗn hợp gồm Fe và Al
tác dụng với dung dịch chứa Cu2+ và 0,03 mol Ag+. Sau
phản ứng thu được hỗn hợp hai kim loại có khối lượng 6,44 gam. Khối lượng mỗi
kim loại có trong hỗn hợp đầu là
A. 1,12 gam và 0,81 gam. B. 0,85 gam và 1,08 gam.
C. 1,39 gam và 0,54 gam. D. 0,56 gam và 1,37 gam.
Câu 36: Cho 1,93 gam hỗn hợp gồm Fe và Al
tác dụng với dung dịch chứa Cu2+ và 0,03 mol Ag+. Sau
phản ứng thu được 6,44 gam hỗn hợp có 2 kim loại. Phần trăm khối lượng Fe trong
hỗn hợp đầu là
A. 58,03% B.
44,04% C. 72,02% D. 29,01%
Câu 37: Cho m gam Mg vào dung dịch có 0,12
mol FeCl3 sau phản ứng hoàn toàn thu được 3,36 gam chất rắn. Giá trị
của m là:
A. 2,16 B. 4,32 C. 5,04 D. 2,88
Câu 38: Cho 5,1 gam hỗn hợp bột gồm Mg và Al có tỉ lệ mol 1:1 vào 150 ml dung dịch hỗn hợp chứa
AgNO3 1M, Fe(NO3)3 0,8M,
Cu(NO3)2 0,6M sau khi các phản ứng xảy ra hoàn toàn thấy
có m gam rắn xuất hiện. Giá trị của m là:
A. 22,68 B. 24,32 C. 23,36 D. 25,26
Câu 39: Cho 13,8 gam hỗn hợp bột Fe và Cu vào 750
ml dung dịch AgNO3 nồng độ x mol/l, sau phản ứng kết thúc thu được
dung dịch X và 37,2 gam chất rắn Y. Cho dung dịch NaOH dư vào dung dịch X thu
được kết tủa, lấy kết tủa nung trong không khí đến khối lượng không đổi được 12
gam hỗn hợp gồm oxit của hai kim loại. Giá trị của x là
A. 0,3 B. 0,4 C. 0,5 D. 0,46
Câu40: Cho 12,19 gam hỗn hợp chứa Al và Fe vào
dung dịch chứa 0,12 mol Fe(NO3)3 và 0,2 mol Cu(NO3)2.
Kết thúc phản ứng thu được dung dịch X chứa 2 muối và rắn Y. Cho Y vào dung
dịch HCl loãng dư thu được 2,016 lít khí H2 (đktc). Dung dịch X tác
dụng với dung dịch NaOH dư, lấy kết tủa nung ngoài không khí đến khối lượng
không đổi thu được m gam rắn khan. Giá trị m
là
A. 14,80 gam B. 12,40 gam C. 19,03
gam D. 21,43 gam
Câu 41: Cho m gam hỗn hợp X gồm bột Fe và Cu có tỉ
lệ khối lượng tương ứng là 7:8 vào 200 ml dung dịch AgNO3 2M, sau
một thời gian phản ứng thu được 52 gam hỗn hợp chất rắn A và dung dịch Y. Lọc
tách X, rồi thêm 32,5 gam bột Zn vào Y, sau khi phản ứng xảy ra hoàn toàn thu
được 46,7 gam chất rắn Z. Để hòa tan hết m gam hỗn hợp X bằng dd HNO3
tạo sản phẩm khử duy nhất là NO thì cần số mol HNO3 tối thiểu là
A. 1,6. B. 2. C. 1,06. D. 0,53.
Câu 42: Cho m gam Fe vào 1 lít dung dịch
hỗn hợp gồm H2SO4 0,1M; Cu(NO3)2
0,1M, Fe(NO3)3 0,1M . Sau khi các phản ứng xảy ra hoàn
toàn , thu được 0,69m gam hỗn hợp kim loại , dung dich X và khí NO (là sản phẩm khử duy nhất ). Giá trị m và
khối lượng chất rắn khan thu được khi cô cạn dung dich X lần lượt là
A. 20
gam va 78,5 gam. B. 20 gam va 55,7 gam.
C. 25,8 gam va 78,5 gam. D. 25,8 gam va 55,7 gam.
Câu 43: Cho 14 gam bột Fe vào 400 ml dung
dịch X gồm: AgNO3 0,5M và Cu(NO3)2 xM. Khuấy
nhẹ cho tới khi phản ứng kết thúc thu được 30,4 gam chất rắn Y và dung dịch Z.
Cho Z tác dụng với dung dịch NaOH dư thì thu được kết tủa một hidroxit kim
loại. Giá trị của x là :
A. 0,1. B. 0,125. C. 0,2. D. 0,15.
Câu 44: Cho 9,2 gam hỗn hợp X gồm Mg, Fe và Cu tác
dụng với 130 ml dung dịch Cu(NO3)2 1M thu được 12,48 gam
chất rắn Y và dung dịch Z. Cho toàn bộ chất rắn Y tác dụng với một lượng dư
dung dịch HCl thu được 0,896 lít H2 (đktc). Cho dung dịch Z tác dụng
với NaOH dư, lọc kết tủa nung trong không khí đến khối lượng không đổi thu được
m gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 7,60. B. 10,80. C. 7,12. D. 8,00.
Câu 45: Cho 13,25 gam hỗn hợp gồm Al và Fe vào 500
ml dung dịch Cu(NO3)2 0,75M và Fe(NO3)3
0,4M thu được dung dịch X và m gam rắn Y. Cho dung dịch NaOH dư vào dung dịch
X, lấy kết tủa nung ngoài không khí đến khối lượng không đổi thu được 20,0 gam
oxit duy nhất. Giá trị m là.
A. 24,0
gam B. 21,2 gam C. 26,8
gam D. 22,6 gam
Câu 46: Dung dịch X gồm AgNO3 và Cu(NO3)2
có cùng nồng độ mol. Lấy một lượng hỗn hợp gồm 0,03 mol Al và 0,05 mol Fe cho
vào 100ml dung dịch X cho tới khi phản ứng kết thúc thu được chất rắn Y chứa
3kim loại. Cho Y vào dung dịch HCl dư giải phóng 0,07 gam khí. Nồng độ mol của
2 muối là:
A. 0,3 M B. 0,4 M C. 0,42 M D. 0,45 M
Câu 47: Cho 300 ml dung
dịch AgNO3 vào
200 ml dung dịch Fe(NO3)2
sau khi phản ứng kết thúc thu
được 19,44 gam chất rắn và dung dịch X trong đó số mol của Fe(NO3)3 gấp đôi số
mol của Fe(NO3)2 còn dư.
Dung dịch X có
thể hoà tan tối đa bao nhiêu gam hỗn hợp bột
kim loại gồm Al và Mg (tỉ
lệ mol 1 : 3) là
A. 11,88 gam. B. 7,92
gam. C. 8,91 gam. D. 5,94 gam.
Câu 48: Cho m gam Mg vào 100 ml dung dịch
chứa CuSO4 0,1M và FeSO4 0,1M. Sau khi phản ứng hoàn toàn
được dung dịch X chứa 2 ion kim loại. Thêm NaOH dư vào dung dịch X được kết tủa
Y. Nung Y ngoài không khí đến khối lượng không đổi được chất rắn Z nặng 1,2
gam. Giá trị của m là:
A. 0,24. B. 0,36. C. 0,48. D. 0,12.
Câu 49: Cho m gam bột Fe vào 200 ml dung
dịch X chứa hỗn hợp AgNO3 và Cu(NO3)2. Khi
phản ứng xong thu được 3,44 gam chất rắn Y và dung dịch Z. Tách Y rồi cho dung
dịch Z tác dụng với dung dịch NaOH dư thì được 3,68 gam kết tủa hai hiđroxit
kim loại. Nung kết tủa trong không khí đến khối lượng không đổi được 3,2 gam
chất rắn. Giá trị của m và nồng độ mol của Cu(NO3)2 trong
dung dịch X lần lượt là:
A. 1,68; 0,05M.
B. 1,68; 0,15M.
C. 0,56; 0,05M.
D. 1,12; 0,15M.
Câu 50: Cho
hỗn hợp ở dạng bột gồm Al và Fe vào 200 ml dung dịch CuSO4 0,525M.
khuấy kỹ hỗn hợp để các phản ứng xảy ra hoàn toàn, sau hản ứng thu được 7,84
gam chất rắn A gồm hai kim loại. Để hòa tan hoàn toàn lượng chất rắn A cần dùng
ít nhất bao nhiêu ml dung dịch HNO3 2 M. biết rằng giải phóng NO là
sản phẩm khử duy nhất?
A. 200ml
B. 180ml
C. 90ml
D. Kq khác
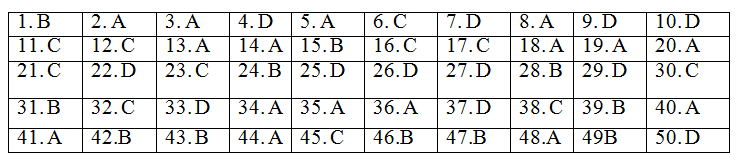
Phần 4. Đáp án và lời giải chi tiết