A - Kiến thức trọng tâm
I. Tính chất hóa học của oxit
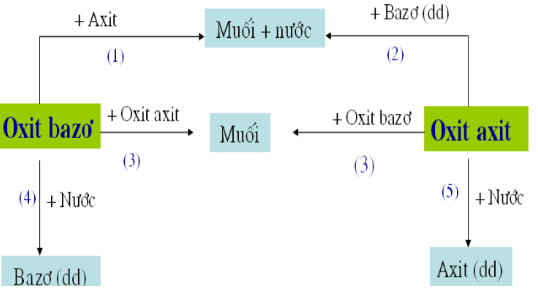
Ví dụ:
(1) CaO + 2HCl → CaCl2 + H2O
(2) CO2 + Ca(OH)2 → CaCO3 + H2O
(3) CaO + CO2 → CaCO3
(4) CaO + H2O → Ca(OH)2
(5) SO2 + H2O →H2SO3
II. Tính chất hóa học của axit
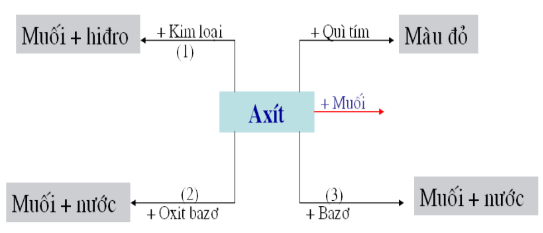
Ví dụ:
(1) H2SO4,loãng + Fe → FeSO4 + H2
(2) H2SO4,loãng + CuO → CuSO4 + H2O
(3) H2SO4,loãng + 2NaOH → Na2SO4 + 2H2O
H2SO4 đặc có tính chất hóa học riêng
- Tác dụng với kim loại không giải phóng khí hidro
- Tính háo nước.Thí dụ khi cho axit H2SO4 vào đường, đường sẽ hóa thành than.
B. BÀI TẬP VÀ HƯỚNG DẪN GIẢI
Bài 1.(Trang 21 SGK)
Có những oxit sau: SO2, CuO, Na2O, CO2. Hãy cho biết những oxit nào tác dụng được với
a) Nước
b) Axit clohiđric
c) Natri hiđroxit
Viết các phương trình hóa học.
Hướng dẫn giải
a) Tác dụng với nước
SO2 + H2O → H2SO3
Na2O + H2O → 2NaOH
CO2 + H2O → H2CO3
b) Tác dụng với HCl
CuO + 2HCl → CuCl2 + H2O
Na2O + 2HCl → 2NaCl + H2O
c) Tác dụng với NaOH
SO2 + 2NaOH → Na2SO3 + H2O
CO2 + 2NaOH → Na2CO3 + H2O
Bài 2.(Trang 21 SGK)
Những oxit nào dưới đây có thể điều chế bằng
a) phản ứng hóa hợp ? Viết phương trình hóa học
b) phản ứng hóa hợp và phản ứng phân hủy ? viết phương trình hóa học.
(1) H2O;
(2) CuO;
(3) Na2O;
(4) CO2;
(5) P2O5
Hướng dẫn giải
a) 5 oxit đã cho đều có thể điều chế bằng phản ứng hóa hợp
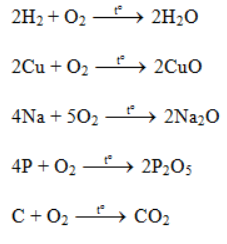
b) Các oxit CuO, CO2, H2O có thể được điều chế bằng phản ứng phân hủy
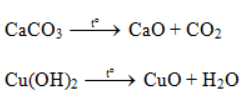
Bài 3.(Trang 21 SGK)
Khí CO được dùng làm chất đốt trong công nghiệp, có lẫn tạp chất là các khí SO2 và CO2. Làm thế nào có thể loại bỏ được những tạp chất ra khỏi CO bằng hóa chất rẻ tiền nhất ?
Viết các phương trình hóa học
Hướng dẫn giải
Do Ca(OH)2 là bazơ và rẻ tiền nên ta dùng Ca(OH)2 để hấp thụ SO2 và CO2
Dẫn hỗn hợp khí đi qua dung dịch Ca(OH)2 dư, toàn bộ SO2 và CO2 bị hấp thụ hết do có phản ứng:
CO2 + Ca(OH)2 → CaCO3 + H2O
SO2 + Ca(OH)2 → CaSO3 + H2O
Khí CO không phản ưng, thoát ra và được thu lấy.
Bài 4.(Trang 21 SGK)
Cần phải điều chế một lượng muối đồng (II) sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric ?
a) Axit sunfuric tác dụng với đồng (II) oxit
b) Axit sunfuric đặc tác dụng với kim loại đồng.
Giải thích các Bài trả lời.
Hướng dẫn giải
a) Axit sunfuric tác dụng với đồng (II) oxit
H2SO4 + CuO → CuSO4 + H2O (1)
b) Axit sunfuric đặc tác dụng với kim loại đồng.
2H2SO4 đ/n + Cu → (to) CuSO4 + SO2 + 2H2O (2)
Ta thấy: để sản xuất ra 1 mol CuSO4 p.ư 1 cần 1 mol H2SO4, p.ư 2 cần 2 mol
Phản ứng (1) tiết kiệm H2SO4 hơn
Bài 5.(Trang 21 SGK)
Hãy thực hiện những chuyển đổi hóa học sau bằng cách viết những phương trình hóa học. (Ghi điều kiện của phản ứng nếu có)
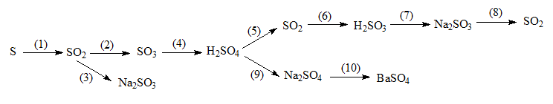
Hướng dẫn giải
(1) S + O2 → SO2 (đk: to)
(2) 2 SO2 + O2 →2 SO3 (đk: to, V2O5)
(3) SO2 + Na2 O → Na2SO3
(4) SO3 +H2O → H2SO4
(5) 2H2SO4 (đ) + Cu → CuSO4 + SO2↑ +2 H2O (đk: to)
(6) SO2 + H2O → H2SO3
(7) H2SO3 + 2 NaOH → Na2SO3 + 2H2O
(8) Na2SO3 + 2HCl → 2 NaCl + SO2 ↑ + H2O
(9) H2SO4 + 2 NaOH → Na2SO4 + 2H2O
(10) NaSO4 + BaCl2 → BaSO4 ↓ + 2 NaCl
C. BÀI TẬP TRẮC NGHIỆM
Câu 1: Cho cùng một lượng sắt và kẽm tác dụng hết với axit clohiđric:
A. Lượng H2 thoát ra từ sắt nhiều hơn kẽm.
B. Lượng H2 thoát ra từ kẽm nhiều hơn sắt.
C. Lượng H2 thu được từ sắt và kẽm như nhau.
D. Lượng H2 thoát ra từ sắt gấp 2 lần lượng H2 thoát ra từ kẽm.
Câu 2: Phản ứng giữa dung dịch Ba(OH)2 và dung dịch H2SO4 (vừa đủ) thuộc loại:
A. Phản ứng trung hoà
B. Phản ứng thế.
C. Phản ứng hoá hợp
D. Phản ứng oxi hoá – khử.
Câu 3: Để nhận biết 3 ống nghiệm chứa dung dịch HCl , dung dịch H2SO4 và nước ta dùng:
A. Quì tím, dung dịch NaCl
B. Quì tím, dung dịch NaNO3.
C. Quì tím, dung dịch Na2SO4
D. Quì tím, dung dịch BaCl2







