A. KIẾN THỨC:
I. TÍNH CHẤT CỦA HIDRO:
1. Tính chất vật lí:
+ Hidro là chất khí không màu, không mùi, không vị.
+ Nhẹ nhất trong các khí (.png) ), tan rất ít trong nước.
), tan rất ít trong nước.
2. Tính chất hóa học:
a) Tác dụng với oxi:
- Khí H2 cháy trong không khí với ngọn lửa nhỏ.
- Khí H2 cháy mãnh liệt trong oxi với ngọn lửa xanh mờ.
Kết luận: H2 tác dụng với oxi sinh ra H2O, phản ứng gây nổ
2H2 + O2 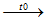 2H2O
2H2O
Tỉ lệ:.png)
+ Khi đốt cháy hỗn hợp H2 và O2 theo tỉ lệ 2:1 sẽ gây nổ mạnh nhất.
b) Tác dụng với đồng oxit:
H2 + CuO 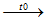 Cu + H2O
Cu + H2O
(màu đen) (màu đỏ)
Nhận xét: Khí H2 đã chiếm nguyên tố O2 trong hợp chất CuO. Khí H2 có tính khử.
Kết luận: Ở nhiệt độ thích hợp, H2 không những kết hợp được với đơn chất O2 mà còn có thể kết hợp với nguyên tố oxi trong 1 số oxit kim loại. Các phản ứng này đều toả nhiều nhiệt.
Ví dụ: H2 + PbO 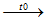 Pb + H2O
Pb + H2O
Fe2O3 + 3H2 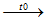 2Fe + 3H2O
2Fe + 3H2O
II. ỨNG DỤNG:
- Bơm kinh khí cầu
- Sản xuất nhiên liệu.
- Hàn cắt kim loại, khử oxi của một số oxit kim loại.
- Sản xuất amoniac, axit, phân đạm....
III. ĐIỀU CHẾ HIDRO.
1. Trong phòng thí nghiệm:
- Khí H2 được điều chế bằng cách: cho axit (HCl, H2SO4(l)) tác dụng với kim loại (Zn, Al, Fe, …)
- Phương trình hóa học:
Zn + 2HCl.png) ZnCl2 + H2
ZnCl2 + H2
- Nhận biết khí H2 bằng que đóm đang cháy.
- Thu khí H2 bằng cách:
+ Đẩy nước.
+ Đẩy không khí.
2. Trong công nghiệp:
Điện phân nước
2H2O .png) 2H2 + O2.
2H2 + O2.
IV. PHẢN ỨNG THẾ:
Ví dụ: Zn + 2HCl .png) ZnCl2 + H2
ZnCl2 + H2
2Al + 3H2SO4.png) Al2(SO4)3 + 3H2
Al2(SO4)3 + 3H2
(đ.chất) (h.chất) (h.chất) (đ.chất)
=> Phản ứng này được gọi là phản ứng thế.
Kết luận: Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của 1 nguyên tố trong hợp chất.
Ví dụ: Trong những phản ứng sau, phản ứng nào là phản ứng thế ? Hãy giải thích sự lựa chọn đó ?
a. 2Mg + O2 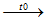 2MgO
2MgO
b. KMnO4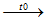 K2MnO4 + MnO2 + O2
K2MnO4 + MnO2 + O2
c. Fe + CuCl2 .png) FeCl2 + Cu
FeCl2 + Cu
d. Mg(OH)2 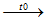 MgO + H2O
MgO + H2O
e. Fe2O3 + H2 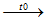 Fe + H2O
Fe + H2O
g. Cu + AgNO3 .png) Ag + Cu(NO3)2
Ag + Cu(NO3)2
V. NƯỚC:
1. Thành phần hóa học của nước:
- Sự phân hủy nước:
2H2O .png) 2H2 + O2.
2H2 + O2.
- Sự hóa hợp nước:
2H2 + O2 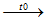 2H2O
2H2O
* Kết luận:
- Nước là hợp chất tạo bởi 2 nguyên tố: H & O.
- Tỉ lệ hoá hợp giữa H & O:
+ Về thể tích: .png)
 + Về khối lượng:
+ Về khối lượng: .png)

- CTHH của nước: H2O.
2. Tính chất vật lí:
Nước là chất lỏng, không màu, không mùi và không vị, sôi ở 1000C, khối lượng riêng 1 g/ml. Hoà tan nhiều chất: rắn, lỏng, khí…
3. Tính chất hóa học:
a) Tác dụng với kim loại:
2Na + 2H2O .png) 2NaOH + H2
2NaOH + H2
Bazơ
Nước có thể tác dụng với một số kim loại mạnh khác như K, Ca, Ba...
b) Tác dụng với một số oxit bazơ.
CaO + H2O .png) Ca(OH)2. (bazơ)
Ca(OH)2. (bazơ)
Nước cũng hóa hợp Na2O, K2O, BaO... tạo NaOH, KOH
Þ Dung dịch bazơ làm đổi màu quì tím thành xanh.
c) Tác dụng với một số oxit axit.
P2O5 + 3H2O .png) 2H3PO4 (axit).
2H3PO4 (axit).
Nước cũng hóa hợp nhiều oxit khác như SO2, SO3, N2O5... tạo axit tương ứng.
Þ Dung dịch axit làm đổi màu quì tím thành đỏ.
VI. AXIT:
1- khái niện: Phân tử axít gồm một hay nhiều nguyên tử hiđrô liên kết với gốc axít, các nguyên tử hiđrô này có thể thay thế bằng các nguyên tử kim loại.
Ví dụ: HCl, H2SO4, HNO3, H3PO4
2. Công thức của axít. HnA
- n: là chỉ số của nguyên tử H
- A: là gốc axít (-Cl, = SO3, = SO4, = S, - NO3,  PO4)
PO4)
3. Phân loại axít.
-Axit không có oxi: HCl, H2S.
-Axit có oxi: HNO3, H2SO4, H3PO4 …
4. Gọi tên của axít.
a. Axít có oxi: Tên axit = axit + PK + ic
Ví du: HNO3 axit nitric ; H2SO4 axit sunfuric
H3PO4 axit photphoric H2CO3 axit cacbonic.
b. Axít không có oxi: Tên axit = axit + PK + hiđic
Ví dụ: H2S axit sunfuhidric.
HCl axitclohiđríc
HBr axit bromhiđic.
c. Axít có ít oxi: Tên axit = axit + PK + ơ
Ví dụ: H2SO3 axit sunfurơ
VII. BAZƠ
1. Khái niệm về bazơ
Bazơ là một phân tử gồm một nguyên tố kim loại liên kết một hay nhiều nhóm hiđroxit (OH ).
Ví dụ: NaOH, Ca(OH)2; Mg(OH)2; Fe(OH)3,
2. Công thức bazơ: M(OH)n
- M: là nguyên tố kim loại
- n:là chỉ số của nhóm (OH )
3. Phân loại bazơ
-Bazơ tan ( kiềm), tan được trong nước
Ví dụ: NaOH; Ca(OH)2, KOH, Ba(OH)2...
-Bazơ không tan, không tan được trong nước.
Ví dụ: Fe(OH)3; Cu(OH)2, Mg(OH)2, ..
4. Cách đọc tên bazơ
Tên bazơ = Tên kim loại (nếu kim loại có nhiều hoá trị gọi tên kèm theo tên hoá trị) + hiđroxit.
Ví dụ: Ca(OH)2 Canxi hidroxit
Fe(OH)2 sắt (II) hidroxit; Fe(OH)3 sắt (III) hidroxit
VIII. MUỐI:
1. Khái niệm: Phân tử muối gồm có một hay nhiều nguyên tử kim loại liên kết một hay nhiều gốc axít.
Ví dụ: NaCl, K2CO3, NaH2PO4, BaCO3, Na2SO4, Na2HPO4, K2SO4, Fe(NO3)3
2. Công thức hoá học của muối:
MxAy. Trong đó: - M: là nguyên tố kim loại.
- x: là chỉ số của M.
- A: Là gốc axít
- y: Là chỉ số của gốc axít.
3.Cách đọc tên muối:
Tên muối = tên kim loại ( kèm hoá trị kim loại có nhiều hoá trị) + tên gốc axít.
4. Phân loại muối:
a. Muối trung hoà: Là muối mà trong gốc axít không có nguyên tử “ H” có thể thay thế bằng nguyên kim loại.
VD: ZnSO4; Cu(NO3)2…
b. Muối axít: Là muối mà trong đó gốc axít còn nguyên tử “H” chưa được thay thế bằng nguyên tử kim loại.
VD: NaHCO3; Ca(HCO3)2…
Bài tập: Trong các muối sau muối nào là muối axit, muối nào là muối trung hoà?
NaH2PO4, BaCO3, Na2SO4, Na2HPO4, K2SO4, Fe(NO3)3
B. BÀI TẬP ÁP DỤNG:
Câu 1: Hoàn thành các phản ứng hoá học và cho biết trong các phản ứng đó thuộc loại phản ứng nào đã học.
|
1/ S + O2 - - - > SO2 3/ CaO + CO2- - - > CaCO3 5/ CaCO3 - - - > CaO + CO2 7/ Fe2O3 + CO - - - > Fe + CO2 |
2/ Fe + CuSO4 - - - >FeSO4 + Cu 4/ KMnO4 - - - > K2MnO4 + MnO2 + O2 6/ CuO + H2 - - - > Cu + H2O 8/ P + O2 - - - > P2O5 |
Câu 2: Hoàn thành các PTPứ hoá học của những phản ứng giữa các chất sau:
|
a/ Mg + O2 - - - >……… b/ Na + H2O - - - >………… c/ P2O5 + H2O - - - >………… |
d/ H2O - - - >………… + …… đ/ KClO3 - - - >……… + ……… e/ Fe + CuSO4 - - - > ……… + ……… |
Câu 3: Viết phương trình hoá học biểu diễn các biến hoá sau và cho biết mỗi phản ứng đó thuộc loại phản ứng nào?
a/ Na .png) Na2O
Na2O .png) NaOH
NaOH
b/ P .png) P2O5
P2O5 .png) H3PO4
H3PO4
c/ KMnO4 .png) O2
O2 .png) CuO
CuO .png) H2O
H2O .png) KOH
KOH
d/ CaCO3 .png) CaO
CaO .png) Ca(OH)2
Ca(OH)2 .png) CaCO3
CaCO3
Câu 4: Cho các CTHH sau: Al2O3, SO3, CO2, CuO, H2SO4, KOH, Ba(OH)2, ZnSO4, Na2SO4, NaHCO3, K2HPO4, Ca(HSO4)2, H3PO4, CaCl2. Hãy cho biết mỗi chất trên thuộc loại hợp chất nào? Gọi tên từng hợp chất.
Câu 5: Có 3 bình đựng riêng biệt các chất khí: Không khí, O2, H2. Bằng cách nào nhận biết được các chất trong mỗi lọ.
Câu 6: Có 4 lọ mất nhãn đựng riêng biệt : dd axit HCl, dd bazơ NaOH, dd muối ăn NaCl, nước cất. Bằng cách nào nhận biết được các chất trong mỗi lọ.
Câu 7: Có 3 bình đựng riêng biệt các dung dịch trong suốt sau: dd NaOH, dd axit HCl, dd Ca(OH)2. Bằng phương pháp hoá học hãy nhận biết mỗi dung dịch đã cho?
Câu 8. Hoàn thành các sơ đồ phản ứng sau:
a) H2O.png) H2 + O2
H2 + O2
b) O2 + P.png) P2O5
P2O5
c) H2 +` Fe2O3 .png) Fe + H2O
Fe + H2O
d) Na + H2O ------>
e) K2O + H2O ------> KOH
g) SO3 + H2O ------> H2SO4
i) Fe + HCl ----> FeCl2 + H2
k) CuO + H2 ----> Cu + H2O
l) Fe + O2 ---> Fe3O4
m) KNO3 ---> KNO2 + O2.
n) Al + Cl2 ---> AlCl3
Câu 9: Viết công thức hoá học của những chất có tên gọi dưới đây:
a) Canxi oxit : …………. Natri oxit ………. kalioxit:…………………
magiê oxit: ……………nhôm oxit:……………. sắt ( II) oxit : …………………..
b)Bari hiđroxit : ………….. Natri hiđroxit: ………........ Kẽmhiđroxit:…………
c) Axit phôtphoric : …………… Axit sunfuric : …………… Axit nitric:…………….
Axit Clohiđric:…………….....Axit sunfurơ: ………………………….
BÀI TOÁN:
Bài 1: Khử 12 g Sắt (III) oxit bằng khí Hiđro.
- Tính thể tích khí Hiđro (ở đktc) cần dùng.
- Tính khối lượng sắt thu được sau phản ứng.
Bài 2. Cho 19,5g Zn tác dụng với dung dịch axitsunfuric loãng.
a) Tính khối lượng kẽm sunfat thu được sau phản ứng.
b) Tính thể tích khí Hiđro thu được ở (đktc).
c) Nếu dùng toàn bộ lượng hiđrô bay ra ở trên đem khử 16g bột CuO ở nhiệt độ cao thì chất nào còn dư? dư bao nhiêu gam?
Bài 3: Hoà tan 7,2 g magie bằng dung dich axit clohiđric
- Thể tích khí H2 sinh ra (đktc)?
- Nếu dùng thể tích H2 trên để khử 19,2 g sắt (III) oxit thì thu được bao nhiêu gam sắt?
Bài 4: Cho 60,5 g hỗn hợp gồm hai kim loại Zn và Fe tác dụng với dung dịch axit clohđric. Thành phần phần trăm của sắt trong hỗn hợp là 46,28%. Hãy xác định:
- Khối lượng mỗi kim loại trong hỗn hợp?
- Thể tích khí H2 sinh ra (ở đktc).
- Khối lượng các muối tạo thành sau phản ứng .
Bài 5: Cho 22,4 g sắt tác dụng với dd H2SO4 loãng chứa 24,5 g H2SO4
- Tính thể tích khí H2 thu được ở đktc?
- Chất nào thừa sau phản ứng và thừa bao nhiêu gam?
Bài 6: Đốt cháy 2,8 lit khí hiđro trong không khí
- Tính thể tích và khối lượng của khí oxi cần dùng?
- Tính khối lượng nước thu được (Thể tích các khí đo ở đktc).
Bài 7: Cho 22,4 lit khí hiđro tác dung với 16,8 lit khí oxi . Tính khối nước thu được. (các khí đo ở đktc).
Bài 8: Khử hoàn toàn 48 gam đồng (II) oxit bằng khí H2 ở nhiệt độ cao
- Tính số gam đồng kim loại thu được?
- Tính thể tích khí H2 (đktc) cần dùng?
Bài 9: Cho một hỗn hợp chứa 4,6 g natri và 3,9 g kali tác dụng với nước .
- Tính thể tích khí hiđro thu được (đktc ) ?
- Tính nồng độ phần trăm của dung dịch biết khối lượng nước là 91,5 g?
Bài 10: Trong phòng thí nghiệm người ta điều chế khí Hiđro bằng cách cho 97,5g kẽm tác dụng với dung dịch Axit clohiđric vừa đủ .
-
- Viết phương trình hoá học của phản ứng xảy ra .
- Tính thể tích khí Hiđro thu được (ở đktc).
- Dẫn toàn bộ lượng khí sinh ra bột đồng (II) oxit dư đun nóng . Tính lượng đồng kim loại tạo thành .
Bài 11: Cho 0,54g Al tác dụng với dung dịch HCl .
- Viết phương trình phản ứng xảy ra.
- Khối lượng đồng tạo thành là bao nhiêu gam?
- Tính thể tích khí hidro thu được (ở đkt.
Bài 1 2: Cho sơ đồ phản ứng: Al + HCl .png) AlCl3 + H2
AlCl3 + H2
a) Hoàn thành sơ đồ phản ứng trên.
b) Nếu có 10,8 gam nhôm đã phản ứng thì thu được bao nhiêu lít khí hidro (ở đktc)?
c) Tính khối lượng muối tạo thành ?







