BÀI TẬP AMIN-AMINO AXIT
Câu
1: Số đồng phân cấu tạo của amin bậc
1 có công thức phân tử ${{C}_{4}}{{H}_{11}}N$
là :
A. 4 B. 2 C. 5 D. 3
Câu
2: Số lượng đồng phân amin chứa vòng
benzen có công thức phân tử ${{C}_{7}}{{H}_{9}}N$ là:
A.4 B. 5 C. 6 D. 8
Câu
3: có bao nhiêu đồng phân có công thức
phân tử là \[{{C}_{2}}{{H}_{7}}{{O}_{2}}N\]vừa tác dụng với HCl vừa tác dụng với
NaOH
A.1 B.2 C.3 D.4
Câu
4: Cặp ancol và amin nào sau đây cùng
bậc:
A.(CH3)3C-OH và (CH3)3C-NH2
B. ${{\left( C{{H}_{3}}
\right)}_{2}}CH-OH$ và ${{\left( C{{H}_{3}} \right)}_{2}}CH-N{{H}_{2}}$
C. ${{C}_{6}}{{H}_{5}}-CH\left( OH
\right)-C{{H}_{3}}$ và ${{C}_{6}}{{H}_{5}}-NH-C{{H}_{3}}$
D. ${{C}_{6}}{{H}_{5}}C{{H}_{2}}-OH$ và $C{{H}_{3}}-NH-{{C}_{2}}{{H}_{5}}$
Câu
5: Cho các chất ${{C}_{4}}{{H}_{10}}O;{{C}_{4}}{{H}_{9}}Cl;{{C}_{4}}{{H}_{10}};{{C}_{4}}{{H}_{11}}N$.
Số đồng phân của các chất giảm theo
thứ tự là:
A.${{C}_{4}}{{H}_{11}}N;{{C}_{4}}{{H}_{10}}O;{{C}_{4}}{{H}_{9}}Cl;{{C}_{4}}{{H}_{10}}$
B.${{C}_{4}}{{H}_{10}}O;{{C}_{4}}{{H}_{11}}N;{{C}_{4}}{{H}_{10}};{{C}_{4}}{{H}_{9}}Cl$
C.${{C}_{4}}{{H}_{10}}O;{{C}_{4}}{{H}_{9}}Cl;{{C}_{4}}{{H}_{11}}N;{{C}_{4}}{{H}_{10}}$
D.${{C}_{4}}{{H}_{10}}O;{{C}_{4}}{{H}_{9}}Cl;{{C}_{4}}{{H}_{10}};{{C}_{4}}{{H}_{11}}N$
Câu 6: Metylamin được coi là dẫn suất của
A.
Metan B. Amoniac C. Benzen D. Nito
Câu
7: Amin có %N về khối lượng là 15,05%
là:
A. ${{\left( C{{H}_{3}} \right)}_{2}}NH$
B. ${{C}_{2}}{{H}_{5}}N{{H}_{2}}$
C. $\left( C{{H}_{3}} \right){}_{3}N$
D. ${{C}_{6}}{{H}_{5}}N{{H}_{2}}$
Câu
8: Khẳng định nào sau đây luôn luôn
đúng:
A. Phân tử khối của một amin đơn chức
luôn là số lẻ.
B. Phân tử khối của một amin đơn chức
luôn là số chẵn.
C. Đốt cháy hết a mol amin bất kì luôn
thu được tối thiểu a/2 mol N2 (phản ứng cháy chỉ cho N2)
D. A và C đúng.
A. Có khả
năng nhận proton
B. Xuất phát
từ amoniac.
C. Phản ứng
được với dung dịch axit.
D. Trên N
còn có 1 đôi electron tự do có khả năng nhận H+
Câu 10: Có 4 hợp chất chứa Nito : amoniac
(X) ; đimetylamin (Y) ; phenylamin (Z) ; metylamin (T). các hợp chất đó được sắp
xếp theo tính bazo tang dần là:
A. Z<><>
C
Z<><>
Câu 11: Dãy gồm các chất đều làm quỳ tím ẩm chuyển sang màu xanh là:
A.anilin,
metylamin, amoniac B.amoni
clorua, metylamin, natrihidroxit
C.anilin,
amoniac, natrihidroxit
D.metylamin, amoniac, natriaxetat
Câu 12: Đốt cháy hoàn toàn 5,9 gam một đơn
chức X thu được 6,72g CO2; 1,12l N2 và 8,1g H2O. Tìm công thức phân tử
A.${{C}_{3}}{{H}_{7}}N{{O}_{2}}$ B.${{C}_{3}}{{H}_{9}}N$ C.${{C}_{2}}{{H}_{7}}N$ D.${{C}_{2}}{{H}_{5}}N{{O}_{2}}$
Câu 13: Đốt cháy hoàn toàn m(g) amin đơn chức
X thu được 9,9 g nước, 10.08 lít hỗn hợp khí CO2 và N2 (đktc) có tỷ khối so với
không khí=1,456. Tìm m và X?
A.${{C}_{2}}{{H}_{7}}N$và 3,7g B.${{C}_{2}}{{H}_{7}}N$và 7,3g
C.${{C}_{4}}{{H}_{11}}N$
và 7,3g D.${{C}_{4}}{{H}_{11}}N$và
3,7g
Câu 14: đốt cháy hoàn toàn 0,25 mol hỗn hợp 2 amin no là đồng đẳng kế tiếp nhau. Sản phẩm cháy được hấp thụ vào bình đựng $Ba{{(OH)}_{2}}$dư xuất hiện 167,45 g kết tủa và khối lượng dung dịch giảm 108g. Tìm công thức phân tử của 2 amin đó?
A.${{C}_{3}}{{H}_{9}}N$
và ${{C}_{3}}{{H}_{9}}N$ B.${{C}_{3}}{{H}_{9}}N$
và ${{C}_{4}}{{H}_{11}}N$
C.${{C}_{3}}{{H}_{9}}N$
và ${{C}_{4}}{{H}_{9}}N$ D.${{C}_{2}}{{H}_{7}}N$
và $C{{H}_{5}}N$
Câu 15: Đốt cháy hoàn toàn m gam một amin X
bằng một lượng không khí vừa đủ thu được 17,6 gam $C{{O}_{2}}$; 12,6 gam ${{H}_{2}}O$
và 69,44 lít khí ${{N}_{2}}$ (đktc).giả thiết không khí chỉ gồm ${{O}_{2}}$ và ${{N}_{2}}$,
trong đó ${{O}_{2}}$ chiếm 20% thể tích không khí. Tìm CTPT của X?
A.${{C}_{2}}{{H}_{7}}N$ B.${{C}_{3}}{{H}_{9}}N$ C.${{C}_{4}}{{H}_{11}}N$ D.${{C}_{4}}{{H}_{9}}N$
Câu 16: Hỗn hợp X gồm 1 mol amino axit no, mạch hở và 1 mol
amin no mạch hở. X có khả năng phản ứng tối đa với 2 mol HCl hoặc 2 mol NaOH. Đốt
cháy hoàn toàn X thu được 6 mol CO2, x mol H2o và y mol N2.
Các giá trị x, y tương ứng là.
A. 8 và 1,0 B. 8 và 1,5 C. 7 và 1,0 D. 7 và 1,5
Câu 17: Hỗn hợp X gồm một số amino axit no ( chỉ có nhóm chức
–COOH và -NH2 không có nhóm chức khác) có tỉ lệ khối lượng mO :
mN = 192 : 77. Để tác dụng vừa
đủ với 19,62 gam hỗn
hợp X cần 220ml dung
dịch HCl 1M. Mặt khác đốt cháy 19,62 gam hỗn hợp X cần V lít O2 (đktc) thu được 7,28 gam CO2.
V có giá trị là.
A. 17,472 B. 16,464 C. 16,576 D. 16,686
Câu 18: Lấy 9,1 gam hợp chất A có công thức
phân tử là C3H9O2N tác dụng với dung dịch NaOH
dư , đun nóng, có 2,24 lít(đktc) khí B thoát ra làm xanh giáy quỳ tím ẩm. đốt
cháy hết lượng khí B nói trên thu được 4,4g CO2 .Công thức cấu tạo của
A và B là:
A.CH2=CHCOONH4 và NH3
B.HCOONH3C2H5
và C2H5NH2
C.HCOONH3C2H3
và C2H3NH2
D.CH3COONH3CH3 và CH3NH2
Câu 19: Hỗn hợp X gồm metylamin; etylamin
và propylamin có tổng khối lượng 21,6 gam và tỷ lệ về số mol là 1:2:1. Cho hỗn
hợp trên tác dụng với HCl thu được bao nhiêu gam muối?
A.12,93
gam B.12,39 gam C.39,12 gam D.39,21 gam
Câu 20: Cho 20g hỗn hợp gồm 3 amin no, đơn
chức, tác dụng vừa đủ với dung dịch HCl 1M. Cô cạn dung dịch thu được 31,68 gam
muối. Thể tích dung dịch HCl đã dùng là
bao nhiêu?
A.250ml B.300ml C.320ml D.350ml
Câu 21: Để kết tủa hết 400ml dung dịch HCl
0,5M và \[FeC{{l}_{3}}\]$$0,8M cần bao nhiêu gam hỗn hợp metylamin và etylamin có tỷ khối
so với hidro là 17,25.
A.40
gam B.40,01
gam C.40,02 gam D. 40,03 gam
Câu 22: Cho sơ đồ chuyển hóa sau:
\[Me\tan \to {{X}_{1}}\to
{{X}_{2}}\to {{X}_{3}}\to {{X}_{4}}\to ani\operatorname{li}n\]
Công thức cấu tạo của các chất hữu cơ
X2;X3;X4 là:
A.\[{{C}_{6}}{{H}_{6}},\,{{C}_{6}}{{H}_{5}}Cl,\,{{C}_{6}}{{H}_{5}}ONa\]
B.\[{{C}_{6}}{{H}_{12}}{{O}_{6}},\,{{C}_{6}}{{H}_{6}},\,{{C}_{6}}{{H}_{5}}N{{O}_{2}}\]
C.\[C{{H}_{2}}=C{{H}_{2}},\,{{C}_{6}}{{H}_{6}},\,{{C}_{6}}{{H}_{5}}N{{H}_{3}}Cl\]
D.\[{{C}_{6}}{{H}_{6}},\,{{C}_{6}}{{H}_{5}}N{{O}_{2}},\,{{C}_{6}}{{H}_{5}}N{{H}_{3}}Cl\]
Câu
23: Phản ứng nào sau đây là đúng:
A.\[{{C}_{2}}{{H}_{5}}N{{H}_{2}}+HN{{O}_{2}}+HCl\to
{{C}_{2}}{{H}_{5}}{{N}_{2}}^{+}C{{l}^{-}}+2{{H}_{2}}O\]
B.\[{{C}_{6}}{{H}_{5}}N{{H}_{2}}+HN{{O}_{2}}+HCl\xrightarrow{0-{{5}^{0}}}{{C}_{6}}{{H}_{5}}{{N}_{2}}^{+}C{{l}^{-}}+2{{H}_{2}}O\]
C.\[{{C}_{6}}{{H}_{5}}N{{H}_{2}}+HN{{O}_{2}}+HCl\xrightarrow{{}}{{C}_{6}}{{H}_{5}}{{N}_{2}}^{+}C{{l}^{-}}+2{{H}_{2}}O\]
D.\[{{C}_{6}}{{H}_{5}}N{{H}_{2}}+HN{{O}_{2}}+HCl\xrightarrow{0-{{5}^{0}}}{{C}_{6}}{{H}_{5}}OH+{{H}_{2}}O\]
Câu
24: Hỗn hợp X gồm hai muối \[AlC{{l}_{3}}\] và \[CuC{{l}_{2}}\] . Hòa
tan dung dịch X vào nước thu được 200 ml dung dịch A.Sục khí metyl amin tới dư
vào dung dịch A thu được 11,7g kết tủa. Mặt khác cho tư từ dung dịch NAOH tới
dư vào dung dịch A thu được 9,8 gam kết tủa. Nồng độ mol/l của \[AlC{{l}_{3}}\] và \[CuC{{l}_{2}}\]lần lượt
là:
A .0,1M;
0,75M B .0,5M; 0,75M C.0,75M; 0,5M D.0,75M;0,1M
Câu 25: X là một amino axit no chỉ chứa một nhóm -NH2
và một nhóm COOH. Cho 0,89 gam X tác dụng với HCl vừa đủ tạo ra 1,225 gam muối.
Công thức cấu tạo của X.
A. H2NCH2CH2COOH
hoặc CH3CH(NH2)COOH
B. NH2CH2COOH
hoặc CH3CH(NH2)COOH
C. H2NCH2CH2CH2COOH
hoặc CH3CH(NH2)COOH
D. H2NCH2COOH
hoặc CH3CH(NH2)CH2COOH
Câu 26: Hợp chất A là một α –amino axit. Cho 0,01 mol A tác dụng vừa đủ với 80ml dung dịch HCl 0,125M, sau đó cô cạn thu được 1,835 gam muối, mặt khác khi trung hòa 2,94 gam A bằng dùng dịch NaOH vừa đủ thu được 3,82 gam muối. Xác định CTCT của A
A. H2NCH2COOH B. CH3CH2(NH2)COOH
C. H2N(CH2)4CH(NH2)COOH D. HOOC-CH2CH2CH(NH2)COOH
Câu 27: Cho 0,01 mol amino axit A tác dụng vừa đủ với 100ml
dung dịch HCl 0,2M thu được dung dịch B.
Dung dịch B này phản ứng vừa đủ với dung dịch NaOH 0,3M, thu được 2,85
gam muối. Xác định công thức cấu tạo biết A là một amino axit thiết yếu mạch thẳng
có chứa nhóm amin cuối mạch.
A.H2N(CH2)4CH(NH2)COOH B. H2NCH2COOH
C. H2NCH2CH2CH2COOH D. CH3CH(NH2)COOH
Câu 28: Cho 13,05 gam hỗn hợp A gồm axit Glutamic và Lysin vào
175ml dung dịch HCl 1M, được dung dịch B. Dung dịch B phản ứng vừa dủ với 175ml
dung dịch NaOH 2M, phần trăm khối lượng của Glutamic trong hỗn hợp A.
A. 50% B. 25,3% C. 28,16% D. 18,16%
Câu 29: chất X lưỡng tính, có công thức phân tử là C3H9O2N phản ứng với 100ml dung dịch NaOH 1,5M . sau khi phản ứng ,cô cạn dung dịch thu được 16,4 gam chất rắn.Công thức cấu tạo thu gọn của X là:
A.amoni
propionat
B.metylamoni propionate
C.metylamoni
axetat D.amoni axetat
Câu 30: Chất hữu cơ X là một muối axit, có
công thức phân tử là
C4H11O3N
có khả năng phản ứng với cả dung dịch axit và dung dịch kiềm. khi cho X tác dụng
với dung dịch NaOH dư rồi cô cạn thì phần rắn thu được chỉ chứa chất vô cơ. Số
công thức cấu tạo phù hợp với tính chất trên là:
A.1 B.2 C.3 D.4
· Đáp án:
HƯỚNG DẪN GIẢI:
Câu 12: theo
đề bài, ta có: nCO2 =0,3
mol=>mC =3,6 gam
nN2 =0,05 mol=>mN =1,4 gam
nH2O =0,45=> mH
=0,9 gam
từ trên, ta
thấy: mC + mH +mN
=3,6+1,4+0,9 =5,9 gam=>X không có oxi.
Ta có : mC : mH : mN
=$\frac{3,6}{12}:\frac{0,9}{1}:\frac{1,4}{14}$=3 :9 :1
Vậy X
là: C3H9N$\left(
\frac{{{n}_{{{H}_{2}}O}}-{{n}_{C{{O}_{2}}}}}{1,5} \right).73=7,3\,gam$
Câu 13: ta có:
nH2O = 0,55 mol
nhỗn hợp khí
=0,45 mol
gọi công thức
phân tử là CXHYNT
đặt---- số
mol của N2 là x
số mol của CO2 là y
ta có hệ phương trình:
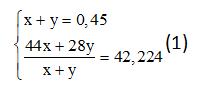
Giải (1) ra, ta được : x= 0,4mol; y=0,05mol
ð x:y:z =4:1:11
vậy công thức phân tử là
C4H11N
mamin=$\left(
\frac{{{n}_{{{H}_{2}}O}}-{{n}_{C{{O}_{2}}}}}{1,5} \right).73=7,3\,gam$
vậy đáp án là C
câu 14: đặt
công thức chung của hỗn hợp là ${{C}_{\overline{n}}}{{H}_{3+2\overline{n}}}N$
ta có : mCO2
+mH2O = m( kết tủa)+ m(dung dịch giảm)
n(kết tủa)=$\frac{167,45}{197}=0,85$
= nCO2=>mCO2= 37,4gam=> mH2O=22,05 gam
ta có : $\overline{n}=\frac{{{n}_{{{H}_{2}}O}}-{{n}_{C{{O}_{2}}}}}{1,5}$=3,4
nên hai chất cần tìm là C3H9N và C4H11N.
câu 15: đặt
công thứ của amin là CXHYN
ta có phương
trình:
CXHYN +$\frac{4x+y}{4}$CO2---> XCO2
+ Y/2 H2O + 0,5N2
Ta có : nCO2=0,4mol ; nH2O=0,7mol ; nN2=3,1mol ; nO2(PU)=0,75mol
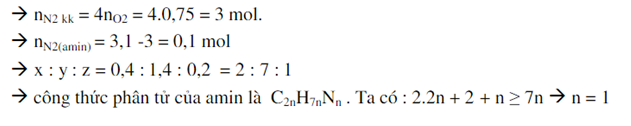
Vậy đáp án
là A
Câu 16: gọi
công thức của amino là R(COOH)X(NH2)Y:
1mol
Công thức của amin là R’NT:
1mol
nHCl=2=y+t=>y=t=1
nNaOH=2mol=>
X=2 mol
ta có công
thức phân tử của amino và amin lần lượt là :CnH2n-1O4N
và CmH2m+3N
phương trình
đốt cháy:CnH2n-1O4N $\xrightarrow{{{O}_{2}}}nC{{O}_{2}}+\frac{2n-1}{2}{{H}_{2}}O+0,5{{N}_{2}}$
CmH2m+3N$\xrightarrow{{{O}_{2}}}mC{{O}_{2}}+\frac{2m+3}{2}{{H}_{2}}O+0,5{{N}_{2}}$
Ta có :
n+m=6; nN2=y=1
nH2O=(2n+1)/2+(2m+3)/2=7
đáp án C
câu 17:
nN=nNH2=nHCl=0,22mol
-->mN=3,08gam;
mO=7,68 gam
-->nO=0,48mol
Ta có nC
=nCO2=0,62mol
Đặt nO2=a
;nH2O=b
mX
=0,62.12+2b+7,68+3,68=19,62
nO=0,48+2a=0,62.2+b
ð a=0,735
ð b=0,71
ð V=22,4a=16,464 lít
Câu 18:
Ta có nA=0,1
mol
nCO2=0,1 mol
=>Chứng tỏ
khí B sinh ra có 1 C. vậy đáp án đúng là D
Câu 19: gọi
số mol của metylamin, etylamin, propylamin làn lượt là X ;2X;X
Ta có :
31.X+ 45.2X+59.X=21,6=> x=0,12 mol
Ta lại có :
nX= nHCl=4X=0,48mol
Áp dụng định
luật bảo toàn khối lượng:
m(muối)=m(amin)+m(axit)=39,12 gam
câu 20: ta
có ptrinh RN+HCl=RNHCl
tương tự, áp
dụng định luật bảo toàn khối lượng
ta tính được
nHCl=0,32 mol
=>VHCl=
320ml
Câu 21:Gọi
công thức hai amin là RNH2
Ta có phương
trình:
RNH2+HCl-->RNH3Cl
3RNH2+FeCl3+3H2O-->Fe(OH)3+3RNH3Cl
Từ hai
phương trình , ta thấy:
$\sum\limits_{{}}^{{}}{{}}$nRNH2=nHCl+3nFeCl3=1,16mol
=>mRNH2=1,16.2.17,25=40,02 gam
Câu 24:
Khi A tác dụng
với metylamin dư có các phản ứng sau:
$3C{{H}_{3}}N{{H}_{2}}+3{{H}_{2}}O+AlC{{l}_{3}}\to
Al{{(OH)}_{3}}+3C{{H}_{3}}N{{H}_{3}}Cl\,\,\,(1)$
$2C{{H}_{3}}N{{H}_{2}}+2{{H}_{2}}O+CuC{{l}_{2}}\to
Cu{{(OH)}_{2}}+2C{{H}_{3}}N{{H}_{3}}Cl\,\,\,(2)$
$4C{{H}_{3}}N{{H}_{2}}+Cu{{(OH)}_{2}}\to
\left[ Cu{{(C{{H}_{3}}N{{H}_{3}})}_{4}} \right]{{(OH)}_{2}}\,\,(3)$
Chỉ thu được
kết tủa là Al(OH)3
Theo (1)
nAlCl3=nAl(OH)3=11,7/78=0,15mol
CM(AlCl3)=0,15/0,2=0,75
M
Tương tự,
khi cho dung dịch A tác dụng với NaOH dư chỉ thu được kết tủa Cu(OH)2
nCuCl2=nCu(OH)2=9,8/98=0,1 mol
CM(CuCl2)=0,1/0,2=0,5M
Câu 26:
Đặt công thức
của A là ${{\left( {{H}_{2}}N \right)}_{a}}R{{\left( \text{COO}H \right)}_{b}}$
Cho A tác dụng
với HCl
${{\left(
{{H}_{2}}N \right)}_{a}}R{{\left( \text{COO}H \right)}_{b}}+aHCl\to {{\left(
Cl{{H}_{3}}N \right)}_{a}}R{{\left( \text{COO}H \right)}_{b}}$
0,01mol 0,01amol 0,01mol
Theo bài ta
có: nHCl=0,08.0,125=0,01=>a=1
=>Mmuối=52,5+R+45b=1,835:0,01=183,5=>
R+45b=131(1)
=>MA=Mmuối-36,5=147
Cho A tác dụng
với NaOH ta có : nA=2,94/147=0,02mol
${{\left( {{H}_{2}}N \right)}_{a}}R{{\left( \text{COO}H \right)}_{b}}+bNaOH\to {{H}_{2}}NR{{(C\text{OO}Na)}_{b}}+b{{H}_{2}}O$
0,02mol 0,02mol
=>Mmuối=16+R+67b=3,82:0,02=191=>R+67b=135(2)
Từ 1 và 2
=>R=41(C3H5)
Vậy đáp án là D
Câu 28: Khi cho B tác dụng với HCl ta coi như:
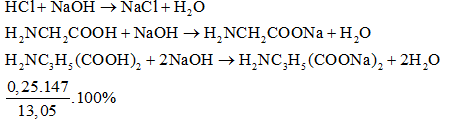
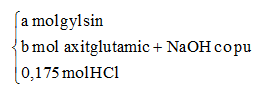
HCl + NaOH--->NaCl
+ H2O
0,175 0,175
${{H}_{2}}NC{{H}_{2}}\text{COO}H+NaOH\to
{{H}_{2}}NC{{H}_{2}}\text{COO}Na+{{H}_{2}}O$
a a a
${{H}_{2}}N{{C}_{3}}{{H}_{5}}{{(C\text{OO}H)}_{2}}+2NaOH\to
{{H}_{2}}N{{C}_{3}}{{H}_{5}}{{(C\text{OO}Na)}_{2}}+2{{H}_{2}}O$
B 2b
Ta có hệ phương trình
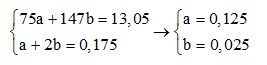
=>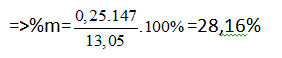
Câu 29: ta
có :nX =0,2 mol
Mmuối=16,4/0,2=82=>CH3COONa
Chất X có
tên là : metylamoni axetat
Câu 30: Từ dữ
kiện đê bài X là muối của axit H2CO3 và ancol dễ bay hơi
và amin khí.
Có 4 đồng
phân phù hợp
HO-COONH-(CH3)3; CH3OCOONH3C2H5;
CH3OCOONH2(CH3)2; C2H5OCOONH3CH3







