A. Tóm tắt lý thuyết
1. Phenol là những hợp chất hữu cơ thu được khi thay thế nguyên tử hidro trong vòng bằng nhóm hidroxyl (OH)
Cần phân biệt phenol và ancol thơm
2. Tính chất hóa học
a) Phản ứng thế nguyên tử H của nhóm –OH: Tác dụng với kim loại kiềm và dung dịch kiềm tạo hợp chất phenolat:
C6H5-OH + NaOH → C6H5-ONa + H2O
C6H5-ONa + CO2 + H2O → C6H5-OH + NaHCO3
So sánh tính axit: CO2 > phenol > HCO3- > ancol.
b) Phản ứng ở vòng benzen
Phenol tác dụng với nước brom tạo tribromphenol kết tủa.
Phản ứng thế vào nhân thơm ở phenol dễ hơn benzen nếu cho phenol phản ứng ở điều kiện êm dịu hơn thì thế được ở các vị trí para và ortho
Dung dịch phenol tác dụng với dung dịch HNO3 cho 2,4,6-trinitrophenol kết tủa màu vàng
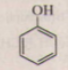 + HNO3 →
+ HNO3 →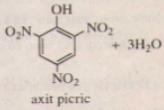 + 3H2O
+ 3H2O
B. BÀI TẬP VÀ HƯỚNG DẪN GIẢI
Câu 1: Trang 193 sgk hóa 11
Ghi Đ (đúng) hoặc S (sai) vào ô trống bên cạnh các câu sau:
a) Phenol C6H5-OH là một rượu thơm
b) Phenol tác dụng được với natri hidroxit tạo thành muối và nước.
c) Phenol tham gia phản ứng thế brom và thế nitro dễ hơn benzen
d) Dung dịch phenol làm quỳ tím hóa đỏ do nó là axit
e) Giữa nhóm –OH và vòng benzen trong phân tử phenol có ảnh hưởng qua lại lẫn nhau.
Hướng dẫn giải
a) S vì rượu thơm là rượu có vòng benzen và nhóm -OH phải gắn vào cacbon no, chứ không gắn trực tiếp vào vòng benzen
b) Đ PTHH: 2C6H5OH + 2NaOH \[\overset{{{t}^{0}}}{\mathop{\to }}\,\] 2C6H5ONa + H2O
c) Đ
d) S vì phenol có tính axit rất yếu nên không làm quỳ tím chuyển sang màu đỏ
e) Đ
Câu 2: Trang 193 sgk hóa 11
Từ benzen và các chất vô cơ cần thiết có thể điều chế được các chất sau:
2,4,6-tribomphenol (1); 2,4,6-trinitrophenol (2).
Viết phương trình hóa học của các phản ứng xảy ra.
Hướng dẫn giải
Từ bezen điều chế 2,4,6-tribomphenol theo sơ đồ sau:
C6H6 → C6H5Br → C6H5ONa → C6H5OH → Br3C6H2OH
(1) Phản ứng thế H trong nhân thơm benzen:
C6H6 + Br2 →(Fe, to) C6H5Br + HBr
(2) Phản ứng thế halogen bằng NaOH:
C6H5Br + NaOH đặc →(to, p) C6H5ONa + HBr
(3) Phản thủy phân muối phenolat :
C6H5ONa + H2O + CO2 → C6H5OH↓ + NaHCO3
(4) Phản ứng thế H trong vòng thơm bằng Br2:
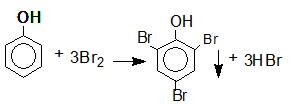
Từ bezen điều chế 2,4,6-trinitrophenol theo sơ đồ sau:
C6H6 → C6H5Br → C6H5ONa → C6H5OH → (NO2)3C6H2OH
(1) Phản ứng thế H trong nhân thơm benzen:
C6H6 + Br2 \[\overset{Fe,{{t}^{0}}}{\mathop{\to }}\,\]C6H5Br + HBr
(2) Phản ứng thế halogen bằng NaOH:
C6H5Br + NaOH đặc \[\overset{p,{{t}^{0}}}{\mathop{\to }}\,\]C6H5ONa + HBr
(3) Phản thủy phân muối phenolat :
C6H5ONa + H2O + CO2 → C6H5OH↓ + NaHCO3
(4) Phản ứng thế H trong vòng thơm bằng HNO3
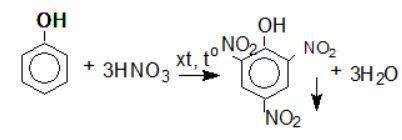
Câu 3: Trang 193 sgk hóa 11
Cho 14,0 gam hỗn hợp A gồm phenol và etanol tác dụng với natri dư thu được 2,24 lít khí hidro (đktc)
a) Viết các phương trình hóa họ c xảy ra.
b) Tính thành phần phần trăm khối lượng của mỗi chất trong A.
c) Cho14,0 gam hỗn hợp A tác dụng với HNO3 thì thu được bao nhiêu gam axit picric (2,4,6- trinitrophenol)?
Hướng dẫn giải
Gọi x và y lần lượt là số mol của C6H5OH và của C2H5OH
a) 2C6H5OH + 2Na → 2C6H5ONa + H2↑
x mol \[\frac{x}{2}\] mol
2 C2H5OH + 2Na → 2C2H5OH + H2↑
y mol \[\frac{y}{2}\]
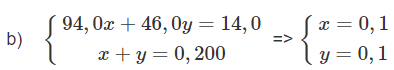
%mphenol = 67,1%; %metanol = 32,9%
c) C6H5OH + 3HNO3 → (NO2)3C6H2OH + 3H2O
\[{{m}_{{{(N{{O}_{2}})}_{3}}{{C}_{6}}{{H}_{2}}OH}}\]= 0,100 x 229 = 22,9 g
Câu 4: Trang 193 sgk hóa 11
Cho từ từ phenol vào nước brom (1) ; stiren vào dung dịch brom trong CCl4 (2). Nêu hiện tượng và viết các phương trình hóa học.
Hướng dẫn giải
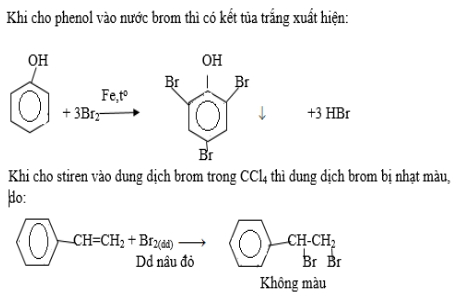
Câu 5: Trang 193 sgk hóa 11
Sục khí CO2 vào dung dịch natri phenolat thấy dung dịch vẩn đục , trong dung dịch có NaHCO3 được tạo thành. Viết phương trình hóa học của phản ứng xảy ra và giải thích. Nhận xét về tính axit của phenol.
Hướng dẫn giải
Phenol là axit yếu nên bị axit cacbonic đẩy ra khỏi dung dịch muối:
C6H5ONa + H2O + CO2→ C6H5OH + NaHCO3
Dung dịch vẩn đục vì có C6H5OH sinh ra
Câu 6: Trang 193 sgk hóa 11
Viết các phương trình hóa học điều chế: phenol từ benzen (1); stiren từ etylbenzen (2). Các chất vô cơ cần thiết coi như có đủ.
Hướng dẫn giải
C6H6 + Br2 \[\overset{Fe,{{t}^{0}}}{\mathop{\to }}\,\] C6H5Br + HBr
C6H5Br + NaOH đặc \[\overset{{{t}^{0}}cao,pcao}{\mathop{\to }}\,\] C6H5ONa + HBr
C6H5ONa + HCl → C6H5OH + NaCl
- Điều chế etylbenzen từ stiren
C6H5CH2CH3 + Br2 2 t0→ C6 C6H5CHBrCH3 + HBr
C6H5CHBrCH3 + KOH \[\overset{{{C}_{2}}{{H}_{5}}OH,{{t}^{0}}}{\mathop{\to }}\,\] C6H5CH=CH2 + KBr
