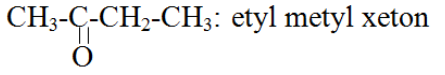A. KIẾN THỨC TRỌNG TÂM
1. Anđehit là những hợp chất hữu cơ mà phân tử có nhóm CH= O liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hidro R(CHO)n.
- Xeton là những hợp chất hữu cơ mà phân tử có nhóm –CO- liên kết trực tiếp với hai nguyên tử cacbon RCOR’
- Danh pháp của anđehit:
+ Danh pháp thay thế: tên của hidrocacbon tương ứng + al
+ Danh pháp thông thường: anđehit + tên axit tương ứng
2. Cấu trúc: Anđehit, xeton đều có nhóm – CO- gọi là nhóm cacbonyl trong phân tử.
Liên kết đôi C=O gồm một liên kết δ và một liên kết π kém bền hơn, tương tự liên kết đôi C=C trong phân tử anken
3. Tính chất hóa học: anđehit, xeton tham gia phản ứng cộng vào nhóm - CO- (cộng H2, H2O, HCN); anđehit dễ bị oxi hóa hơn xeton (anđehit tác dụng với dung dịch bạc nitrat trong ammoniac).
4. Phương pháp điều chế: phương pháp chung để điều chế anđehit là oxi hóa nhẹ ancol bậc 1, điều chế xeton là oxi hóa nhẹ ancol bậc 2 bằng CuO. Các ahđehit và xeton thông thường được sản xuấ từ hidrocacbon như: điều chế HCH=O từ metan, CH3-CH=O từ atilen, CH3-CO-CH3 từ cumen.
B. Bài tập và hướng dẫn giải
Giải bài 1 trang 203 SGK Hóa học 11
Thế nào là anđehit? Viết công thức cấu tạo của các anđehit có công thức phân tử C4H8O và gọi tên chúng.
Hướng dẫn giải
- Định nghĩa: anđehit là những hợp chất hữu cơ mà phân tử có nhóm -CH=O liên kết trực tiếp với nguyên tử cacbon (1) hoặc nguyên tử hiđro
(1) Nguyên tử cacbon này có thể của gốc hidrocacbon hoặc nhóm -CHO
- Các CTCT của anđehit có CTPT C4H8O:
CH3-CH2-CH2-CHO anđehit butyric (butanal).
CH3- CH (CH3)–CHO anđehit isobutiric (2- metyl propanal).
Giải bài 2 trang 203 SGK Hóa học 11.
Viết các phương trình hóa học để chứng tỏ rằng, anđehit vừa có tính oxi hóa vừa có tính khử.
Hướng dẫn giải
CH3CH=O + H2 \[\overset{Ni,{{t}^{0}}}{\mathop{\to }}\,\] CH3CH2OH
Chất oxi hóa Chất khử
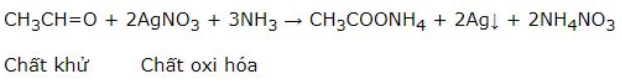
Giải bài 3 trang 203 SGK Hóa học 11.
Hướng dẫn giải
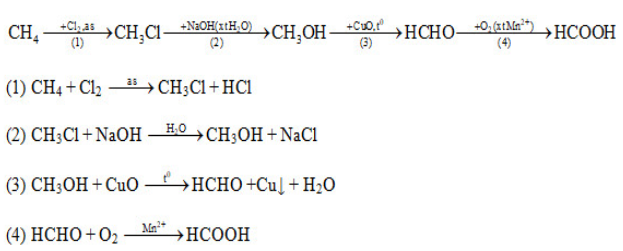
Giải bài 4 trang 203 SGK Hóa học 11.
Cho 1,0 ml dung dịch fomanđehit 5 % và 1,0 ml dung dịch NaOH 10,0 % vào ống nghiệm, sau đó thêm tiếp từng giọt dung dịch CuSO4và lắc đều cho đến khi xuất hiện kết tuả. Đun nóng phần dung dịch phía trên, thấy có kết tủa màu đỏ gạch của Cu2O. Giải thích hiện tượng thí nghiệm và viết phương trình hóa học.
Hướng dẫn giải
- Khi nhỏ dung dịch CuSO4 vào thì có kết tủa xanh xuất hiện:
2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4
- Khi đun nóng phần trên ống nghiệm trên ngọn lửa đèn cồn thì có kết tủa đỏ gạch xuất hiện:
HCHO + 4Cu(OH)2 + 2NaOH → Na2CO3 + 2 Cu2O↓đỏ gạch + 6H2O
Giải bài 5 trang 203 SGK Hóa học 11.
Cho 50,0 gam dung dịch anđehit axetic tác dụng với dung dịch AgNO3 trong NH3 (đủ) thu được 21,6 gam Ag kết tủa. Tính nồng đồ % của anđehit axetic trong dung dịch đã dùng.
Hướng dẫn giải
\[{{n}_{Ag}}=\frac{21,6}{108}=0,2(mol)\]
CH3CH=O + 2AgNO3 + 3NH3 → CH3COONH4 + 2Ag↓ + 2NH4NO3
nCH3CHO = ½ nAg = 0,1 (mol)
%\[{{C}_{C{{H}_{3}}CHO}}=\frac{{{m}_{C{{H}_{3}}CHO}}}{m{{}_{ddC{{H}_{3}}CHO}}}.\]100%\[=\frac{0,1.44}{50}.100\]% =8,8%
Giải bài 6 trang 203 SGK Hóa học 11.
Ghi Đ(đúng) hoặc S (sai) vào ô trống bên cạnh các câu sau:
a) Anđehit là hợp chất chỉ có tính khử.
b) Anđehit cộng hidro tạo thành ancol bậc một.
c) Anđehit tác dụng với dung dịch bạc nitrat trong ammoniac sinh ra bạc kim loại.
d) Anđehit no, đơn chức, mạch hở có công thức phân tử tổng quát CnH2nO.
e) Khi tác dụng với hidro, xeton bị khử thành ancol bậc II.
Hướng dẫn giải
a) S vì andehit có cả tính khử và tính oxi hóa
c) Đ
b) Đ
d) Đ
e) Đ
Giải bài 7 trang 203 SGK Hóa học 11.
Cho 8,0 gam hỗn hợp hai anđehit kế tiếp nhau trong dãy đồng đẳng của anđehit no, đơn chức, mạch hở tác dụng với bạc nitrat trong dung dịch ammoniac (lấy dư) thu được 32,4 gam bạc kết tủa. Xác định công thức phân tử, viết công thức cấu tạo và gọi tên các anđehit.
Hướng dẫn giải
Đặt công thức chung của 2 anđehit là CxH2x+1 CHO
Số mol Ag = 0,300 mol = 2 lần số mol anđehit. Vậy Manđehit = 53,33 g/ mol
14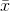 + 30 = 53,33 =>
+ 30 = 53,33 => 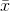 = 1,6. Vậy 2 anđehit là CH3CHO và C2H5CHO
= 1,6. Vậy 2 anđehit là CH3CHO và C2H5CHO
Giải bài 8 trang 204 SGK Hóa học 11.
Oxi hóa không hoàn toàn etilen (có xúc tác) để điều chế anđehit axetic thu được hỗn hợp X. Dẫn 2,24 lít khí X (quy về đktc) vào một lượng dư dung dịch bạc nitrat trong NH3 đến khi phản ứng hoàn toàn thấy có 16,2 gam bạc kết tủa.
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Tính hiệu suất của quá trình oxi hóa etilen.
Hướng dẫn giải
Phương trình phản ứng:
2CH2=CH2 + O2 → 2CH3CHO (1)
Hỗn hợp X gồm: CH2=CH2 và CH3CHO
CH3CHO + 2AgNO3 + 3NH3 → CH3COONH4 + 2Ag↓ + 2NH4NO3 (2)
Theo phương trình (2):
Số mol Ag = 0,150 mol. Vậy số mol CH3CHO = 0,0750 mol
Hiệu suất của quá trình oxi hóa etilen : \[\frac{0,075}{0,1}\]100% = 75%
Bài 9 trang 204 sgk hóa học 11
Hợp chất X no, mạch hở có phần trăm khối lượng C và H lần lượt bằng 66,67% và 11,11% còn lại là O. tỉ số hơi của X so với oxi bằng 2,25
a) Tìm công thức phân tử của X
b) X không tác dụng với dung dịch AgNO3 trong NH3 nhưng khi tác dụng với hidro sinh ra X1. X1 tác dụng được với natri giải phóng hidro. Viết công thức cấu tạo va gọi tên của hợp chất X.
Hướng dẫn:
Đặt CTPT của X là CxHyOz
Ta có x : y : z =\[\frac{66,67}{121}:\frac{11,11}{1}:\frac{22,22}{16}\] = 4 :8 : 1
CTCTĐG : C4H8O
Mx = 2,25 x 32,0 = 72,0 (g/mol)
Vậy CTPT X là : C4H8O
CTCT: